
생화학분자생물학회입니다.
TDP-43 단백질 병증 모델에서 단백질품질조절시스템 손상에 의해 나타나는 신경세포 사멸을 억제하는 새로운 분자기전 (PTK2-TBK1-SQSTM1) 규명
작성자
관리자작성일자
2020-07-17조회수
1370
TDP-43 단백질 병증 모델에서 단백질품질조절시스템 손상에 의해 나타나는 신경세포 사멸을 억제하는 새로운 분자기전 (PTK2-TBK1-SQSTM1) 규명
PTK2/FAK regulates UPS impairment via SQSTM1/p62 phosphorylation in TARDBP/TDP-43 proteinopathies
Autophagy 5:1-17, 2019



이신려 : 한국뇌연구원 치매연구그룹 연구원 (E-mail: srlee@kbri.re.kr)
김기영 : 순천향대학교 의료생명공학과 교수 (E-mail: kiyoung2@sch.ac.kr)
김형준 : 한국뇌연구원 치매연구그룹 책임연구원 (E-mail: kijang1@kbri.re.kr)
연구배경
근위축성 측삭 경화증 (Amyotrophic lateral sclerosis, ALS)은 뇌와 척수에서 운동 뉴런의 진행성 퇴화를 특징으로 하는 치명적인 신경퇴행성 질환으로 (1), 현재 ALS에 대한 FDA승인 약물은 2개뿐이며, 이 약물들도 단지 2 ~ 3개월 정도 생존기간을 연장할 수 있는 것으로 알려졌다 (2). ALS를 포함하는 여러 신경퇴행성 질환에서 공통적으로 나타나는 특징 중 하나는 손상된 뉴런에 유비퀴틴-양성 응집물이 존재하는 것이다 (3, 4). 정상 진핵세포에서 유비퀴틴화 된 단백질이 급속하게 분해되는 것을 고려할 때 (5), ALS의 손상된 뉴런에서 유비퀴틴화 된 단백질 응집물의 축적은 유비퀴틴 프로테아좀 시스템 (ubiquitin proteasome system, UPS)의 활성이 ALS 환자의 운동 뉴런에서 손상될 수 있다는 가능성을 제시한다. 몇몇 ALS 연관유전자 (SQSTM1, VCP, OPTN, 및 UBQLN2)가 UPS 잘못접힌 단백질 분해에 직접으로 관련되어 있다는 점이 이러한 가설을 뒷받침한다 (6). 한편, UPS와 자가포식경로 (autophagy lysosomal pathway, ALP)가 ALS 관련 질환 단백질을 분해할 수 있으며, 이에 따라 질환을 완화시킬 수 있음이 보고된 바가 있다 (7). ALS 환자의 운동뉴런에서 유비퀴틴-양성 응집물의 주요 성분은 TAR DNA binding protein (TDP-43)이다. TDP-43는 진화적으로 잘 보존된 핵 RNA 결합 단백질이며, TDP-43 응집체의 세포질 내 축적은 대부분 ALS환자에서 나타나는 병리학적 특징이다. 또, TDP-43에서 발견되는 50개 이상의 과오 돌연변이 (missense mutation)가 산발성 및 가족력의 ALS에 관련이 있다는 것이 알려져 있다 (8). 특히, TDP-43에 의해 유도된 신경 독성은 현재 ALS 및 TDP-43 응집체 축적과 관련된 다른 신경 퇴행성 질환의 발병에 기여하는 것으로 잘 알려져 있다 (그림1). 그러나 TDP-43 단백질 병증의 신경병리학적 분자기전은 정확하게 알려져 있지 않다. 이에 본 연구진은 TDP-43 단백질 병증 세포 및 초파리 모델을 이용하여 TDP-43 축적이 단백질품질조절시스템 손상을 일으키는 것을 증명하고, 이러한 손상에 의한 신경독성을 억제하는 새로운 분자기전을 발굴하였다.
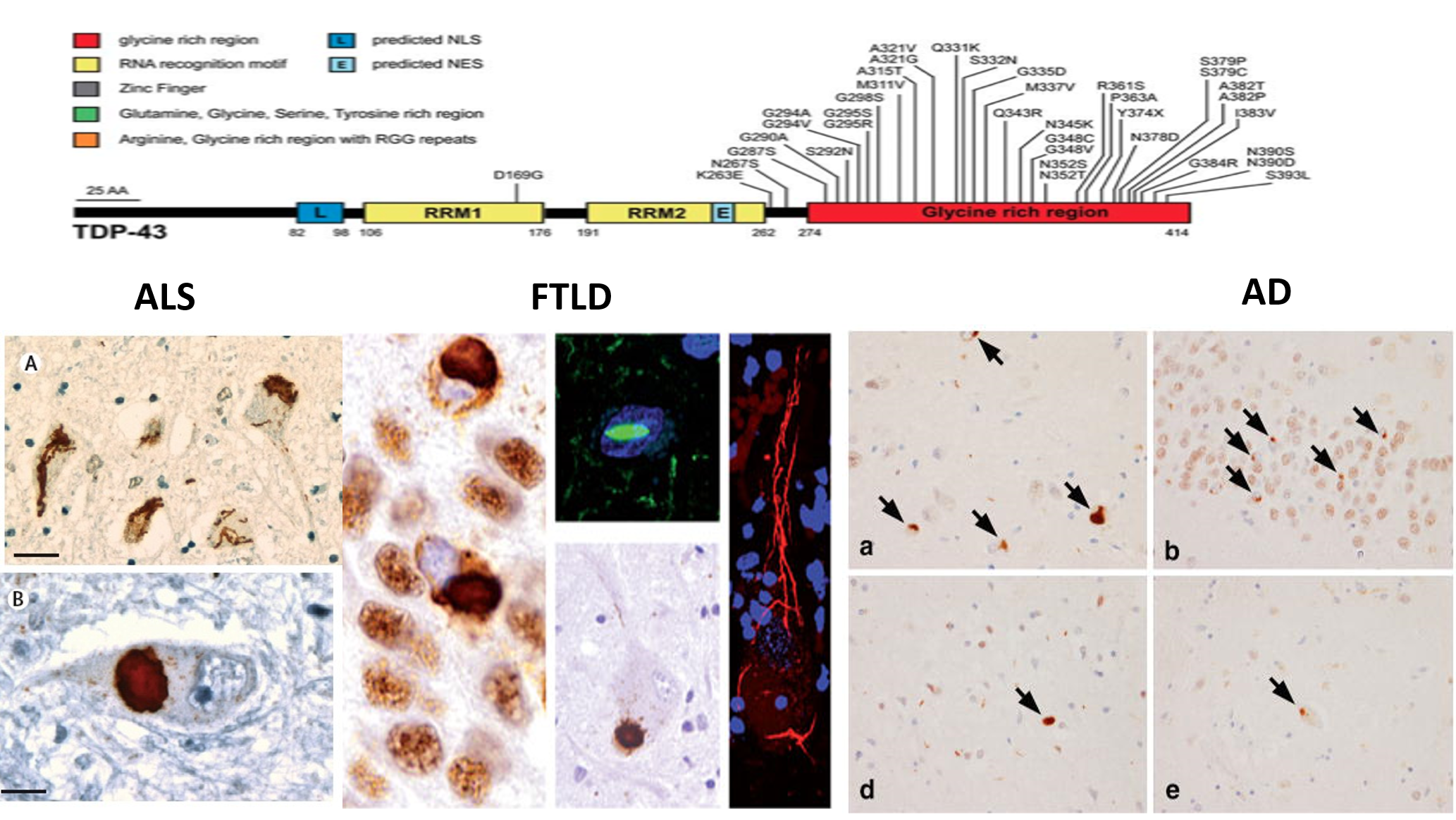
그림1) TDP-43 단백질 구조 및 ALS, FTLS, AD 환자에서 보여지는 TDP-43의 비정상적인 응집.
연구결과
1. TDP-43 단백질 병증 신경세포 모델에서 UPS 손상 확인
불용성 TDP-43의 세포질에서의 축적은 근위축성 측삭 경화증 및 전두 측두엽 치매 (FTLD)와 같은 TDP-43 단백질 병증 모델의 주요 병리학적 특징이며 (9), 이러한 축적은 신경 퇴행을 유발한다 (10). 마우스 신경세포에 human TDP-43을 과발현 시킨 다음 폴리-유비퀴틴화된 단백질의 발현을 관찰한 결과, 불용성 분획에서 폴리-유비퀴틴화된 단백질의 수준이 현저하게 증가되었으며, 핵 및 세포질에서의 TDP-43 단백질 발현이 명확하게 증가된 것을 관찰하였다. 또, UPS 손상 시 활성화된다는 것이 잘 알려져 있는 자가포식-리소좀 경로 (ALP, 11)가 증가되어 있는 것을 관찰하였다 (그림2). 이는 TDP-43 단백질 병증 신경세포 모델에서 UPS의 기능이 약화되어 있다는 것을 의미한다.
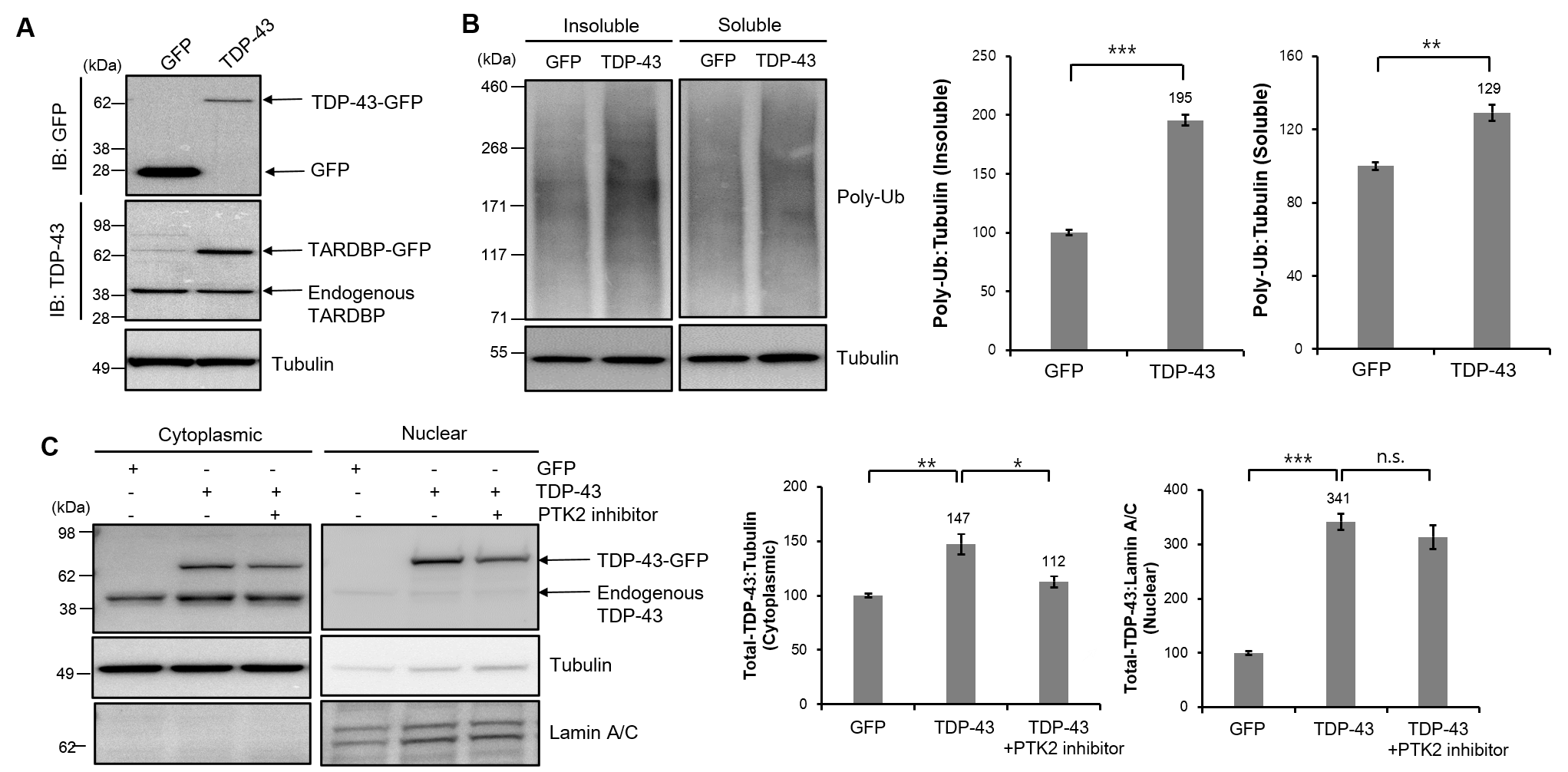
2. TDP-43 단백질 병증 신경세포 및 초파리 모델에서 UPS 손상에서 PTK2의 기능
TDP-43 신경 독성을 억제할 수 있는 인자들을 발굴하기 위하여 키나아제 저해제 (kinase inhibitor, 인산화효소 저해제) 스크리닝을 통해 일반적인 UPS inhibitor인 MG132에 의해 유도되는 세포 독성을 조절하는 분자를 스크리닝한 결과, PTK2/FAK 억제제가 MG132에 의해 유도되는 독성을 상당히 완화시키는 것을 확인하였다. 이러한 PTK2는 세포 이동과 생존에 관련된 다기능성 단백질이다. 이 단백질의 397번째 타이로신기는 (Y397) 자가-인산화를 통해 인산화 되는 것으로 알려져 있어 Y397 인산화 정도를 통해 해당 단백질의 활성 정도를 측정할 수 있다 (12). 그러나, 이 단백질의 단백질품질조절시스템에서의 역할은 현재까지 알려져 있지 않다.
먼저, TDP-43 과발현에 의해 PTK2의 Y397 인산화가 현저히 증가되어 있는 것을 확인하였다. 그리고 PTK2가 TDP-43에 의한 신경 독성을 개선시키는지 확인한 결과, PTK2 억제는 TDP-43 과발현에 의해 유도된 불용성 폴리-유비퀴틴화된 응집체의 축적을 감소시킬 뿐만 아니라, TDP-43에 의해 유도된 세포 사멸도 억제한다는 것을 관찰하였다. 이러한 결과는 PTK2 억제가 TDP-43 병증 신경세포 모델에서 TDP-43에 의해 나타나는 신경 독성을 강하게 완화시킨다는 것을 보여주었다. 또한, 초파리 ALS 모델을 이용하여 in vivo에서 PTK2의 기능을 확인한 결과, 불용성 폴리-유비퀴틴화된 단백질의 양이 TDP-43이 과발현되는 초파리의 신경계에 축적되며, Fak (초파리 PTK2 유사체)의 억제에 의해 TDP-43에 의해 증가되는 불용성 폴리-유비퀴틴화된 단백질의 양이 효과적으로 감소된 것을 관찰하였다. 게다가 Fak이 억제된 초파리에서는 TDP-43이 과발현되는 초파리에서 나타나는 운동능력 및 수명단축이 개선되었다 (그림3). 이러한 결과는 세포 기반 TDP-43 단백질 병증 모델과 유사하게 Fak의 억제가 TDP-43이 발현되는 초파리에서 나타나는 UPS 손상을 억제하고, 이를 통해 TDP-43에 의해 나타나는 신경계의 기능 저하를 억제함을 보여준다.
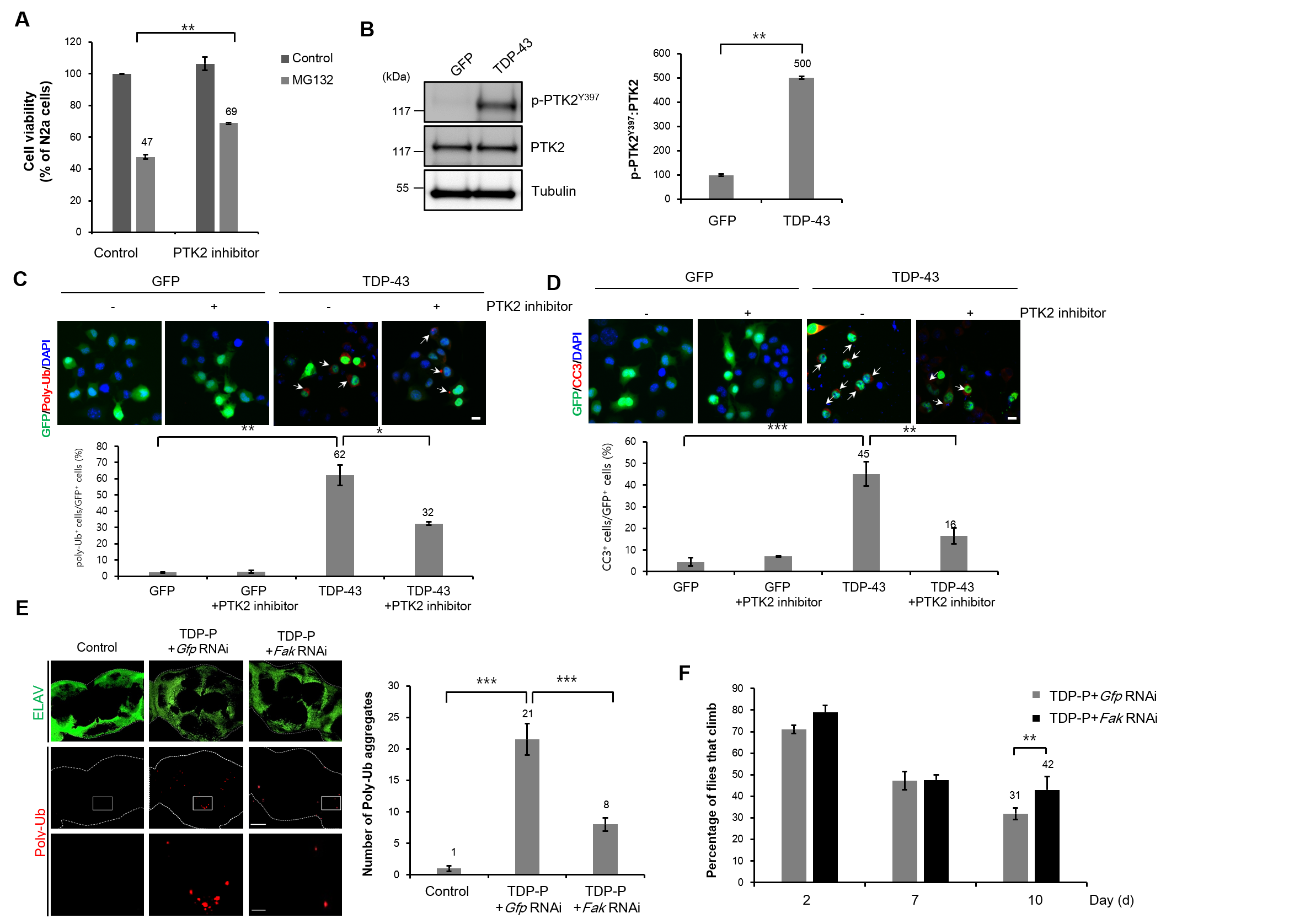
3. TDP-43 단백질 병증 모델에서 단백질 품질 조절 손상에 의해 야기된 신경독성의 새로운 분자기전 연구
PTK2의 저해는 UPS가 억제된 상황 속에서도 불용성 폴리-유비퀴틴화된 단백질의 수준을 현저하게 감소시킬 수 있음을 확인하였다. 이러한 결과는 PTK2 억제가 UPS 이외의 메커니즘에 의해 폴리-유비퀴틴화된 단백질의 분해를 개선시킨다는 것을 시사한다. 폴리-유비퀴틴화된 단백질은 UPS 손상 조건 하에서 ALP에 의해 분해될 수 있으며 (13), SQSTM1/p62은 ALP에 의한 폴리-유비퀴틴화된 단백질의 분해를 매개하는 유비퀴틴 결합 단백질이다 (14). 그리고 SQSTM1의 인산화는 유비퀴틴화된 단백질의 자가포식 소체로의 이동을 조절한다 (15). 이러한 이전 연구 결과들을 바탕으로, 본 연구팀은 SQSTM1의 403번째 세린기의 (S403) 인산화가 UPS 손상에 의해 유발된 신경 독성에 PTK2와의 관련성이 있는 가를 관찰하였다. TDP-43 과발현시 SQSTM1의 S403 인산화가 현저하게 증가되었으며, PTK2 억제가 TDP-43에 의해 증가되는 SQSTM1의 S403 인산화를 효과적으로 감소시켰다. 그리고 리소좀 분해의 특정 억제제인 Bafilomycin A1 (BafA1)을 이용하여 SQSTM1의 S403 탈인산화가 UPS 손상 조건에서 불용성 폴리-유비퀴틴화된 단백질의 자가포식 분해를 개선시키는 것을 추가로 확인하였다. 즉, PTK2가 SQSTM1의 S403 인산화 조절을 통해 TDP-43에 의한 UPS의 기능장애로 유도되는 신경독성을 조절할 수 있음을 확인하였다. PTK2는 타이로신기를 인산화 하는 활성만을 지니고 있으므로 SQSTM1의 세린기를 직접 인산화하는 것은 불가능하다. 추가적인 연구를 통해, PTK2가 UPS 손상 조건 하에서 TBK1이라는 세린-트레오닌 키나아제의 매개를 통해 SQSTM1의 S403 인산화 조절과 신경 세포 독성을 완화함을 확인하였다 (그림4). 이를 통하여 TDP-43가 일으키는 UPS 손상에 의해 유도된 신경 독성을 PTK2-TBK1-SQSTM1 분자기전을 통해 조절하여 TDP-43에 병인에 중요한 역할을 할 가능성을 확인하였다.
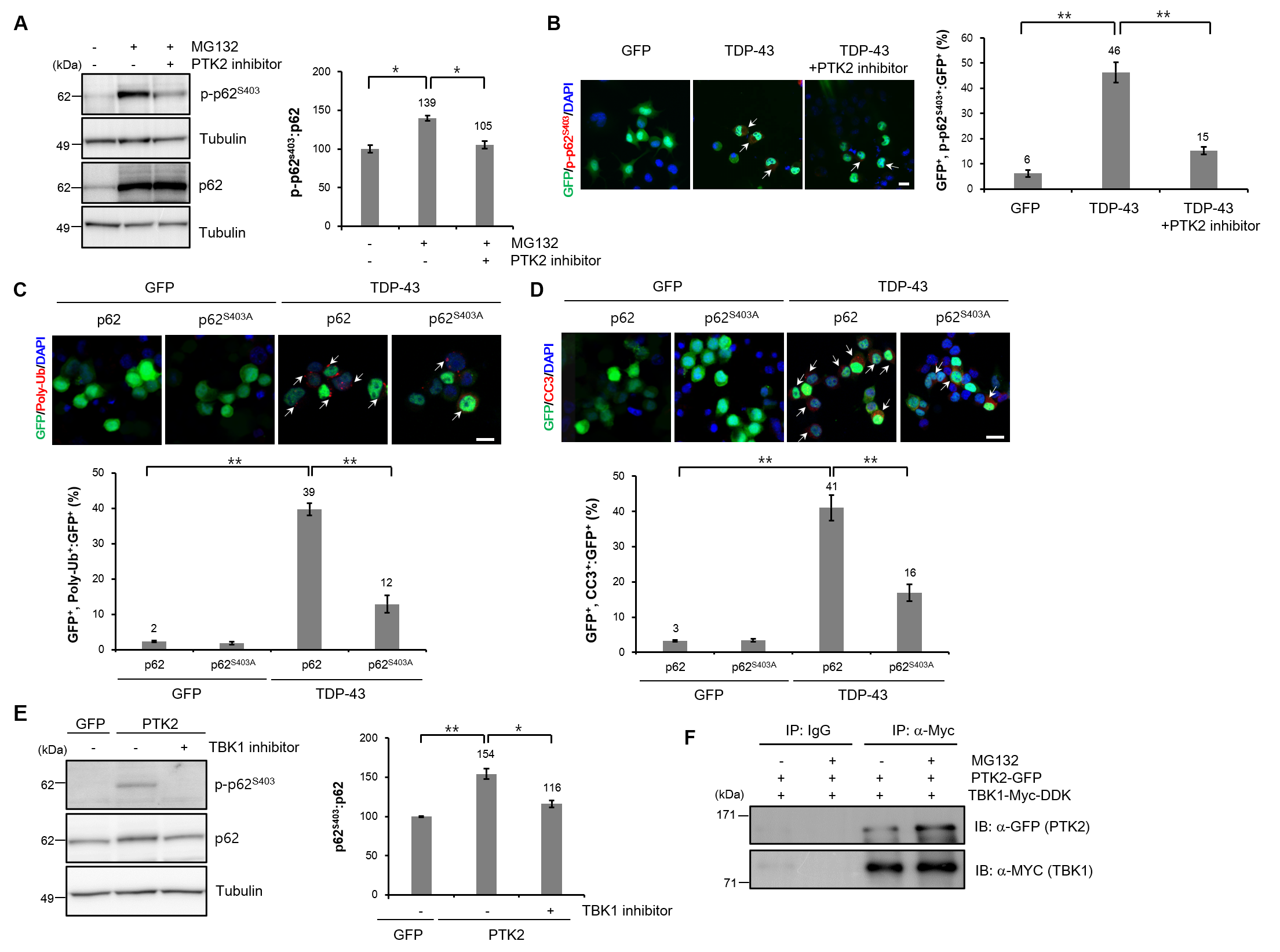
연구의 성과 및 의의
본 연구팀은 TDP-43 단백질 병증 세포 및 초파리 모델에서 TDP-43 과발현에 의해 단백질품질조절에 관여하는 유비퀴틴화된 단백질 분해 능력이 억제된 것을 밝히고, 이것이 TDP-43 신경 독성의 주요 원인임을 검증하였다. 후속 실험을 통해 PTK2 저해는 SQSTM1의 403번째 세린기의 인산화를 억제함으로써, TDP-43 단백질에 의해 유도된 유비퀴틴화된 단백질 감소와 신경 독성 완화를 유도한다는 것을 밝혔다. 게다가 TDP-43에 의한 신경세포 퇴행을 억제할 수 있는 세가지 단백질(PTK2, TBK1, SQSTM1)의 역할을 새롭게 발견하고, 이들의 상호작용이 UPS 손상시 세포내 또 다른 단백질 품질조절시스템인 자가포식 리소좀 경로(ALP)를 조절하여 신경세포의 퇴행 현상을 억제할 수 있음을 증명하였다.
이를 통해 치매와 근위축성 측삭 경화증의 병인 기전중 하나인 TDP-43 단백질에 의한 신경퇴행 증상을 회복시킬 수 있는 새로운 경로의 분자기전을 밝혀냄으로써, 향후 치매와 근위축성 측삭 경화증 환자의 신경세포 내 축적된 비정상 단백질을 제거할 수 있는 새로운 치료 전략을 제시할 수 있을 것으로 기대된다.
참고문헌
(1) Al-Chalabi A, Jones A, Troakes C, et al. The genetics and neuropathology of amyotrophic lateral sclerosis. Acta Neuropathol. 2012;124(3):339-352.
(2) Costa J, Gomes C, de Carvalho M. Diagnosis, pathogenesis and therapeutic targets in amyotrophic lateral sclerosis. CNS Neurol Disord Drug Targets. 2010;9(6):764-778.
(3) Bendotti C, Marino M, Cheroni C, et al. Dysfunction of constitutive and inducible ubiquitin-proteasome system in amyotrophic lateral sclerosis: implication for protein aggregation and immune response. Prog Neurobiol. 2012;97(2):101-126.
(4) Neumann M, Sampathu DM, Kwong LK, et al. Ubiquitinated TDP-43 in frontotemporal lobar degeneration and amyotrophic lateral sclerosis. Science. 2006;314(5796):130-133.
(5) Ross JM, Olson L, Coppotelli G. Mitochondrial and Ubiquitin Proteasome System Dysfunction in Ageing and Disease: Two Sides of the Same Coin? Int J Mol Sci. 2015;16(8):19458-19476.
(6) Lee JK, Shin JH, Lee JE, et al. Role of autophagy in the pathogenesis of amyotrophic lateral sclerosis. Biochim Biophys Acta. 2015;1852(11):2517-2524.
(7)Ciechanover A, and Kwon YT. Degradation of misfolded proteins in neurodegenerative diseases: therapeutic targets and strategies. Exp. Mol. Med. 2015;47(3):e147.
(8) Buratti E. Functional Significance of TDP-43 Mutations in Disease. Adv Genet. 2015;91:1-53.
(9) Meriggioli MN, Kordower JH. TDP-43 Proteinopathy: Aggregation and Propagation in the Pathogenesis of Amyotrophic Lateral Sclerosis. Mov Disord. 2016;31(8):1139.
(10) Scotter EL, Chen HJ, Shaw CE. TDP-43 Proteinopathy and ALS: Insights into Disease Mechanisms and Therapeutic Targets. Neurotherapeutics. 2015;12(2):352-363.
(11) Wang C, Wang X. The interplay between autophagy and the ubiquitin-proteasome system in cardiac proteotoxicity. Biochim Biophys Acta. 2015;1852(2):188-194.
(12) Hanks SK, Ryzhova L, Shin NY, et al. Focal adhesion kinase signaling activities and their implications in the control of cell survival and motility. Front Biosci. 2003;8:d982-996.
(13) Korolchuk VI, Menzies FM, Rubinsztein DC. Mechanisms of cross-talk between the ubiquitin-proteasome and autophagy-lysosome systems. FEBS Lett. 2010;584(7):1393-1398.
(14) Lippai M, Low P. The role of the selective adaptor p62 and ubiquitin-like proteins in autophagy. Biomed Res Int. 2014;2014:832704.
(15) Matsumoto G, Wada K, Okuno M, et al. Serine 403 phosphorylation of p62/SQSTM1 regulates selective autophagic clearance of ubiquitinated proteins. Mol Cell. 2011;44(2):279-289.
첨부파일