
생화학분자생물학회입니다.
Laboratory of Alzheimer’s Disease Research
작성자
관리자작성일자
2017-12-01조회수
787Laboratory of Alzheimer’s Disease Research
묵인희
서울대학교 의과대학 생화학교실
[연구실소개]
서울대학교 의과대학 의과학관에 자리 잡고 있는 알츠하이머병 연구실은 알츠하이머병의 병인기전을 규명하고 이러한 병인기전에 근거한 조기진단 및 치료제 개발의 타깃을 설정하고자 하는 목표를 가지고 연구를 진행하고 있다. 노인성 치매의 70% 정도를 차지하고 있는 알츠하이머병은 인구의 고령화와 더불어 그 환자 수가 폭발적으로 증가하고 있는 Unmet Need의 질병으로 잘 알려져 있다. 현재 국내에만 65세 이상 노인인구 중 10%에 달하는 유병률을 가진 질병으로 조기진단 및 치료제의 개발이 절실한 상황이다. 본 연구팀은 알츠하이머병의 병인기전 연구를 유전자, 단백질, 세포 내의 소기관별 등으로 아주 세분화하여 분자적 기전을 규명하고자 하는 것과 동시에 다양한 알츠하이머병 동물모델을 이용하여 환자에게서 나타나는 여러 가지 in vivo 현상들이 어떤 기전으로 일어나는지를 병리학적 관점으로 연구를 진행하고 있다. 이러한 연구결과들을 토대로 실제 알츠하이머병 환자들의 혈액 샘플 혹은 이미징 결과들을 가지고 임상적 적용이 가능한 부분이 있는지를 보고 치료제 개발의 타깃을 설정하고 조기진단의 혈액 바이오마커들을 규명하는 등의 연구를 수행하고 있다.
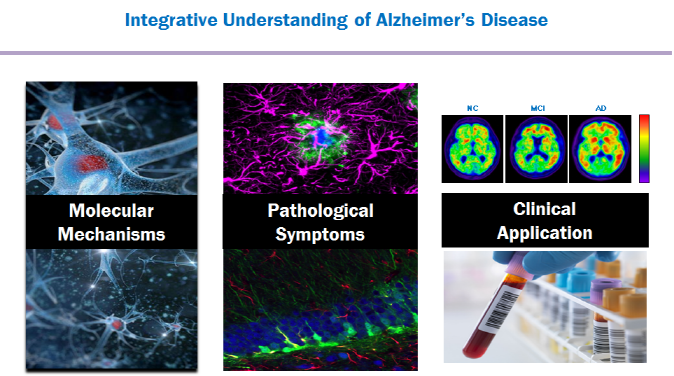
[연구내용]
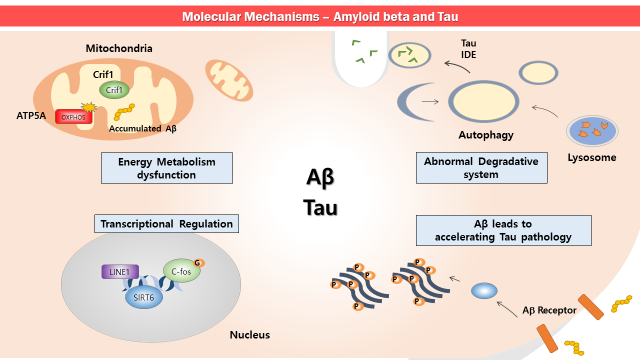
1. 베타아밀로이드와 타우를 중심으로 하는 알츠하이머병의 분자적 병인기전 연구
알츠하이머병의 주요 병인으로 알려진 베타아밀로이드와 타우는 세포 내에서 만들어진 후에 다양한 생리학적 기능을 하기도 하지만 이러한 단백질들의 생성과 분해의 불균형이 초래되면서 세포 내에 많은 변화를 유도하게 된다. 베타아밀로이드는 아밀로이드전구대사단백질(Amyloid Precursor Protein, APP)을 베타시크리테아제와 감마시크리테아제가 순차적으로 자르면서 생기는 40 혹은 42개의 단백질이다. 베타아밀로이드는 노인반(Senile Plaque)을 생성하기 이전에 Soluble Form으로 존재하며 직접 Mitochondria나 ER과 같은 세포 내 소기관에 영향을 주기도 하며 주변의 Microglia나 뇌혈관장벽(Blood Brain Barrier, BBB)을 공격하여 뇌염증반응 등을 일으키기도 한다. 타우 단백질은 신경세포의 축삭돌기(Axon)를 이루는 Microtubule을 안정화시키는 단백질로서 잘 알려져 있으나 알츠하이머병 환자의 경우는 이러한 타우 단백질의 변성이 일어나 축삭돌기의 불안정화를 야기하게 된다. 과거에는 타우 단백질의 변성이 GSK-3β, MAPK, Cdk5, CaMK 등의 다양한 Kinase들에 의한 과인산화가 주된 원인이라고 생각해 왔으나 이러한 과인산화 이외에도 Acetylation, Truncation, Ubiquitination과 같은 다양한 Form의 단백질 수식화 및 대사가 일어나면서 타우 변성을 유도한다고 알려지고 있다. 최근에는 알츠하이머병의 주요 병인이라고 알려진 베타아밀로이드와 타우 사이의 연관관계를 찾고자 하는 많은 연구들이 진행되고 있다. 알츠하이머병 환자의 뇌 영상 기술이 급속하게 발전하면서 베타아밀로이드의 축적은 치매증상 발병 10-20년 전에 나타나고 있고 타우 변성에 의한 Neurofibrillary Tangle은 치매 증상과 연관관계를 보이며 증가한다는 보고와 함께 초기에 축적이 시작된 베타아밀로이드가 타우의 변성에 영향을 미칠 것이 보고되고 있다. 베타아밀로이드와 변성된 타우 단백질의 축적 등은 세포 내 정상적인 단백질 혹은 망가진 소기관의 분해 시스템(Ubiquitin Proteasome System, UPS 혹은 Autophagy)이 Malfunction을 하면서 일어나기도 한다. 단백질이 만들어지고 분해되어 세포내 항상성이 유지되고 있다가 이러한 시스템이 고장이 나면서 만들어지는 단백질들을 제때 분해해내지 못한다면 특정 단백질 혹은 없어져야 할 소기관의 축적이 일어나고 이러한 것들은 세포의 생리에 심각한 영향을 줄 것이다. 또한, 면역시스템과 알츠하이머병과의 상관관계들이 많이 보고되어 있고 뇌 내에서는 Microglia가 이러한 면역기능에 관여한다고 알려져 있다. 정상의 경우에는 Microglia가 Phagocytosis를 하면서 베타아밀로이드의 분해를 유도하지만 과도하게 활성화된 Microglia는 Inflammatory Cytokine을 분비하면서 뇌 내의 염증반응을 유도하기도 한다. 최근에는 이러한 뇌 내의 염증반응들이 혈액 내에 존재하는 Neutrophil이나 Macrophagy, Monocyte 등의 면역관련 세포들과 서로 Cross-Talk을 한다는 보고들이 있다. 이러한 다양한 분자적 병리기전에 근거하여 본 연구실에서는 다음과 같은 연구들을 수행하고 있다.
(0) 베타아밀로이드가 미토콘드리아 기능에 미치는 분자적 병인기전 규명
(1) 베타아밀로이드가 타우변성에 미치는 세포 내 신호전달 및 유전자 발현 체계 규명
(2) 변성되어서 축적된 단백질과 제 기능을 못하는 소기관들의 분해 및 제거 기전 연구(UPS, Autophagy)
(3) Peripheral Immune System과 뇌와의 Cross-Talk 기전 연구
(4) 세포 수준에서뿐만 아닌 다양한 알츠하이머병 동물모델 개발 및 그를 응용한 병리기전 연구
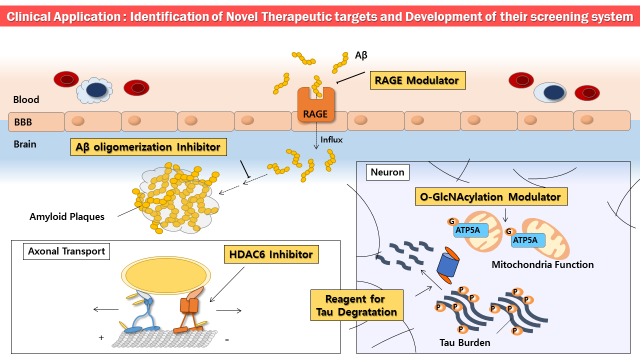
2. 알츠하이머병 치료제 타깃 발굴 및 약물 스크리닝 시스템 개발
알츠하이머병은 현재 증상 완화제만이 존재하고 원인 치료제는 전무한 Unmet Need의 질병이다. 전 세계 다국적 제약회사를 주도로 베타아밀로이드와 타우를 타깃으로 하는 새로운 신약개발이 활발하게 시도되고 있다. 본 연구실에서는 베타아밀로이드와 타우의 병인기전에 연관이 되어 있지만 그것 자체를 타깃으로 하기보다는 이러한 응집, 변성 단백질에 의해서 야기되는 여러 현상의 병인기전을 규명하고 이러한 기전에 근거한 새로운 신약개발의 타깃을 발굴하고자 한다. 뇌혈관장벽(BBB)에 존재하면서 혈액 내의 베타아밀로이드를 뇌 내로 들여보내주는 관문의 역할을 하는 RAGE(Receptor for Advanced Glycation Endproduct)의 Modulator를 스크리닝하는 시스템을 개발하여 베타아밀로이드와 RAGE의 Interaction을 줄여주는 약물을 개발할 수 있게 하였고 이것을 계기로 하여 RAGE의 Downstream Signaling에 PRAK이라는 Kinase가 관여한다는 것을 알게 되었다. 현재 이 기술은 국내 기업을 통해 다국적 제약회사에 기술이전되어 있다. 알츠하이머병의 주요 증상인 인지기능 및 학습능력의 저하는 신경세포의 연결고리인 시냅스의 약화로 인해 나타나고 이러한 시냅스의 약화는 신경세포의 Soma와 Axon Terminal 간의 분자 및 신호의 이동이 원활하지 않은 것이 영향을 주게 된다. 시냅스 말단에서 Synaptic Vesicle의 분비에 필요한 ATP의 공급을 위해서 미토콘드리아가 Axon을 따라서 이동하게 되는데 알츠하이머병 동물모델의 경우나 베타아밀로이드를 배양하는 신경세포에 처리했을 경우 모두 미토콘드리아의 Axonal Transport가 저하되어 나타나는 것이 보고되어 있다. 또한 타우 단백질은 Axonal Transport에 직접적으로 영향을 미치는 것이기에 Axonal Transport에 영향을 주는 분자들을 타깃으로 알츠하이머병의 치료제 타깃을 검증하는 것들이 이루어지고 있다. 본 연구실에서는 HADC6가 Axonal Transport에 연관되어 있는 Tau와 Tubulin 등의 Acetylation에 관여하므로 HDAC6 Inhibitor에 의한 Axonal Transport의 영향을 살펴보고자 한다. 그리고 뇌 내의 당대사의 변화는 알츠하이머병 환자에게서 잘 알려진 사실인데 이러한 당대사의 변화가 분자적 병인기전에는 어떠한 영향을 미칠지에 대한 연구는 많이 보고되어 있지 않다. 본 연구실에서는 O-GlcNAcylation이라는 단백질 수식화 중의 하나에 중점을 두고 알츠하이머병 환자의 경우 O-GlcNAcylation이 어떻게 변화하며 이것이 어떠한 단백질에 영향을 주고 병인기전과는 어떠한 연관관계가 있는지를 규명하고자 한다. O-GlcNAcylation 과정에서 Sugar를 붙여주는 OGT(O-GlcNAc transferase)와 OGA(O-GlcNAcase)와 Interaction하는 기전 또한 살펴보고자 하며 O-GlcNAcylation Modulator를 알츠하이머병 치료제의 타깃으로 설정하고 이를 스크리닝 할 수 있는 시스템을 만들어 나가고 있다. 이상에서와 같이 본 연구실에서 병인기전에 근거한 알츠하이머병의 치료제 타깃을 설정하고 그 스크리닝 시스템을 만들어 가고자 하는 연구들은 다음과 같다.
(0) Tau Degradation Molecule
(1) Tau Aggregation Inhibitor
(2) Abeta Oligomerization Inhibitor
(3) RAGE Modulator
(4) HDAC6 Inhibitor
(5) O-GlcNAcylation Modulator
[연구책임자]

묵인희 교수
주소: 서울특별시 종로구 대학로 103, 서울대학교 의과대학 생화학교실
전화: 02-740-8245
팩스: 02-3672-7352
Homepage: www.alzlab.co.kr
[연구진구성]
교수: 묵인희
연구교수: 한선호(연구부교수), 정은선(연구조교수)
박사후 연구원: 김윤희
박사과정: 강석조, 김동규, 김행준, 박종찬, 백성훈, 최현정, 최희선
석사과정: 서규진, 정선우, 최하영
연구원: 김은혜, 정단비

[대표논문]
1. Choi, H., Kim, H.J., Kim, J., Kim, S., Yang, J., Lee, W., Park, Y., Hyeon, S.J., Lee, D.S., Ryu, H., Chung, J., Mook-Jung, I. (2017) Increased acetylation of Peroxiredoxin1 by HDAC6 inhibition leads to recovery of Aβ-induced impaired axonal transport. Mol Neurodegener 12(1):23.
2. Park, J.C., Han, S.H., Cho, H.J., Byun, M.S., Yi, D., Choe, Y.M., Kang, S., Jung, E.S., Won, S.J., Kim, E.H., Kim, Y.K., Lee, D.Y., Mook-Jung, I. (2017) Chemically treated plasma Aβ is a potential blood-based biomarker for screening cerebral amyloid deposition. Alzheimers Res Ther 9(1):20.
3. Son, S.M., Cha, M.Y., Choi, H., Kang, S., Choi, H., Lee, M.S., Park, S.A., Mook-Jung, I. (2016) Insulin-degrading enzyme secretion from astrocytes is mediated by an autophagy-based unconventional secretory pathway in Alzheimer disease. Autophagy 12(5):784-800.
4. Kwon, H.J., Cha, M.Y., Kim, D., Kim, D.K., Soh, M., Shin, K., Hyeon, T., Mook-Jung, I. (2016) Mitochondria-Targeting Ceria Nanoparticles as Antioxidants for Alzheimer's Disease. ACS Nano 10(2):2860-70.
5. Han, S.H., Park, J.C., Mook-Jung, I. (2016) Amyloid β-interacting partners in Alzheimer's disease: From accomplices to possible therapeutic targets. Prog Neurobiol 137:17-38.