
생화학분자생물학회입니다.
ARD1에 의한 Hsp70 Acetylation에 의해 스트레스로 손상된 단백질이 처리되는 기전 규명
작성자
관리자작성일자
2017-04-01조회수
790ARD1에 의한 Hsp70 Acetylation에 의해 스트레스로 손상된 단백질이 처리되는 기전 규명
ARD1-Mediated Hsp70 Acetylation Balances Stress-Induced Protein Refolding and Degradation Nat Commun 7:12882, 2016



서지혜 박지현 김규원
계명대학교 의과대학 서울대학교 약학대학 서울대학교 약학대학
연구배경
모든 생명체는 외부 환경의 갑작스러운 변화로부터 스스로를 보호하기 위한 방어 체계를 가지고 있다. 세포가 외부의 해로운 환경에 노출되면 스트레스 반응(Stress Response) 이라는 방어 기전을 작동하여 스스로를 보호하는데, 이 기전을 담당하는 단백질들을 Heat Shock Proteins(Hsp)이라 한다. Hsp Family는 분자 크기에 따라 Hsp90, Hsp70, Hsp60 등으로 다양하게 나누어 지는데, 대부분 Molecular Chaperone으로 세포 내의 손상된 단백질들을 처리하는 역할을 한다 (1). Hsp70은 대표적인 Hsp 단백질로 1962년 Ritossa에 의해 열충격(Heat Shock) 후 발현이 증가되는 단백질로 동정되었으며, 이 후 열충격 외에도 pH 변화, 독성 물질, 저산소 등 다양한 종류의 스트레스에 의해 발현이 증가되는 것이 밝혀져 Stress Protein이라고도 불린다 (2). 세포가 스트레스를 받으면 세포 내의 단백질이 손상되어 구조가 변형되는데, 이 때 Hsp70은 두 가지 방법을 통해 손상된 단백질을 처리한다. ⅰ) 첫 번째는 손상된 단백질의 구조를 회복(Refolding) 하여 원래대로 복구시키는 방법이고, ⅱ) 다른 하나는 Proteasome을 통해 손상된 단백질을 분해(Degradation) 하여 세포 내에서 완전히 제거해 버리는 방법이다 (3). Hsp70의 이러한 상반된 기능은 Hop이나 Chip 같은 Co-Chaperone 단백질들에 의해 결정된다. Hop과 Chip은 Hsp70의 C-말단의 동일한 부위에 경쟁적으로 결합하는데, Hop은 Hsp70과 Hsp90을 연결시켜 손상된 단백질의 Refolding을 유도하며, Chip은 Ubiquitin Ligase로 Hsp70과 결합하여 손상된 단백질의 Degradation을 유도하는 역할을 한다 (그림 1) (4).
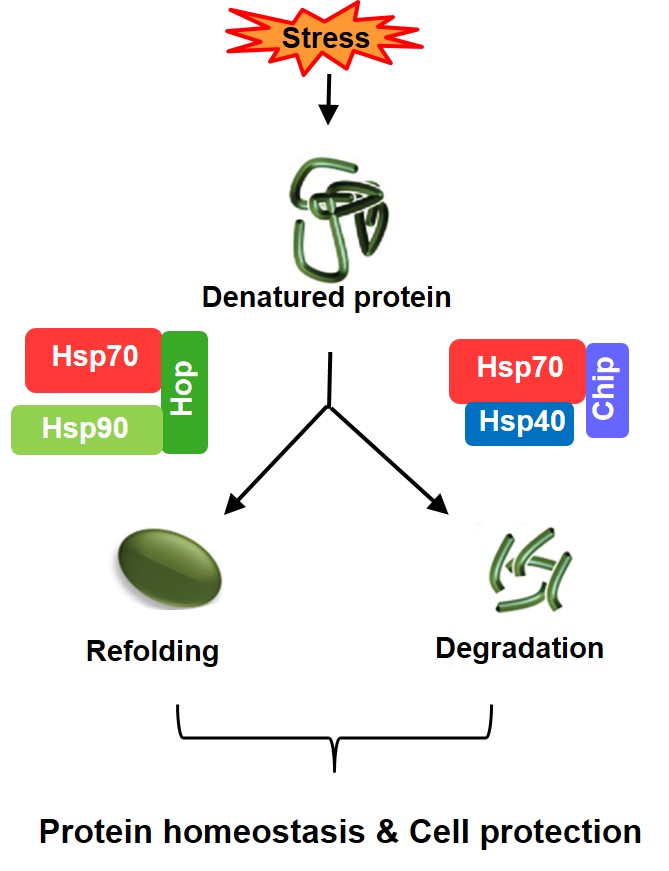
그림 1. 스트레스 후 Hsp70에 의한 손상된 단백질의 처리 방법
Hsp70은 스트레스에 의해 손상된 단백질을 처리하기 위해 단백질 구조를 Refolding 하여 복구하거나 Degradation시켜 세포 내에서 제거한다. Hsp70이 Refolding 또는 Degradation 기능을 수행할 때에는 각각 다른 종류의 Co-Chaperone 단백질들과 협력한다.
이처럼, Hsp70은 손상된 단백질의 "Refolding" 과 "Degradation" 이라는 두 가지 상반된 기전을 통해 세포 내 단백질의 항상성을 유지함으로써 스트레스로부터 세포를 보호한다. 하지만, Hsp70가 이러한 두 가지 상반된 작용을 어떻게 구별하고 선택적으로 조절하는지, 또는 이 두 가지 기능을 상황에 따라 전환할 수 있는 스위치가 존재하는 것인지에 대해서는 전혀 알려진 바가 없다. 따라서, 본 연구에서는 Hsp70의 상반된 기능을 결정하는 분자 기전을 규명하고자 하였다. 최근 Hsp70 단백질이 세포 내에서 Phosphorylation, Acetylation, Methylation 등 다양한 형태로 Post-Translational Modification 되어 있다는 연구 결과들이 발표되었고, 이러한 Modification은 단백질의 기능을 신속하게 전환할 수 있는 스위치 역할을 할 수 있으므로 (5-7), 이에 근거하여 본 연구진은 Hsp70의 상반된 두 기능이 스트레스 상황에서 Post-Translational Modification에 의해 스위치 될 것이라는 가설을 정립하고 연구를 진행하였다.
연구결과
1. 스트레스 상황에서 시간에 따른 Hsp70의 기능 전환 확인
먼저 Hsp70의 Refolding 및 Degradation 기능이 스트레스 상황에서 어떻게 변화되는지를 알아보기 위해 Hsp70의 기능을 결정하는 Co-Chaperone 단백질들의 결합을 조사하였다. 스트레스 초기(1시간, 4시간)에는 손상된 단백질의 Refolding에 관여하는 Hop, Hsp90이 Hsp70에 주로 결합하였고, 후기(12시간, 24시간)로 가면서 단백질 Degradation에 필요한 Chip, Hsp40의 결합이 증가되는 현상을 보였다 (그림 2A). 이는 Hsp70이 스트레스 초기에는 우선 손상된 단백질의 Refolding을 통해 복구 시키려 하고, 이후 지속적인 스트레스로 인해 손상이 누적되어 더 이상 복구가 힘들어지면 손상된 단백질을 Degradation하여 세포 내에서 제거하는 쪽으로 그 기능을 전환한다는 것을 의미한다. 반면, 정상 상황에서의 단백질 합성, 제거를 담당하는 Hsc70의 경우 Hsp70과는 달리 스트레스 이후 Co-Chaperone 단백질 결합에 아무런 변화를 보이지 않았으며 (그림 2A), 이를 통해 Hsp70의 이러한 변화가 스트레스 상황에 특이적으로 반응하는 기전임을 알 수 있었다. 다음은, 이러한 Hsp70의 기능 전환이 Post-Translational Modification에 의해 조절될 가능성을 확인하기 위해 Hsp70의 Acetylation을 조사하였다. 흥미롭게도 Co-Chaperone 단백질들의 결합 변화와 비슷한 패턴으로 Hsp70의 Acetylation이 스트레스 초기에 증가하다가 후기로 갈수록 감소하였으며, 반면 Hsc70의 Acetylation에는 아무런 변화가 없었다. 이러한 결과는 Hsp70의 기능 전환에 acetylation이 연관되어 있을 가능성을 시사한다 (그림. 2B).
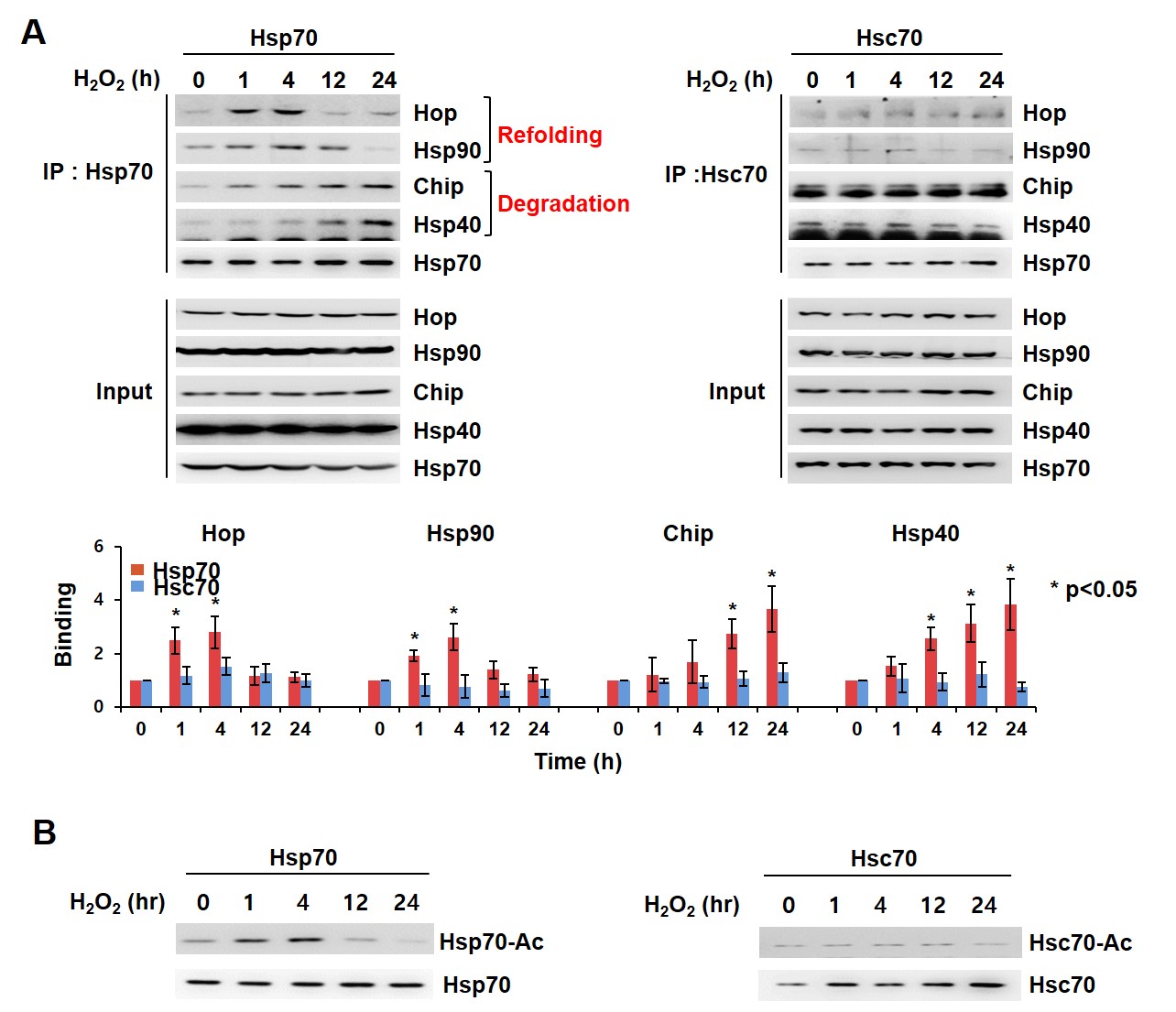
그림 2. Hsp70의 Chaperone 기능과 Acetylation과의 연관성
스트레스 상황에서 Hsp70의 기능 변화를 조사하기 위해 Co-Chaperone 단백질의 결합을 조사하였다. Hsp70은 스트레스 초기(1시간, 4시간)에는 단백질의 Refolding을 담당하다가, 후기(12시간, 24시간)에는 Degradation으로 그 기능을 전환하였다 (A). 그리고 이와 유사한 패턴으로 Hsp70의 Acetylation이 초기에 증가하고 후기에 다시 감소하였다 (B).
2. ARD1에 의한 Hsp70의 K77 Acetylation 확인
다음으로는 스트레스 상황에서 Hsp70의 Acetylation을 매개하는 Acetyltransferase를 동정하고자 하였으며, 그 결과 ARD1이라는 Acetyltransferase가 Hsp70과 결합하여 Hsp70을 직접적으로 Acetylation 시킨다는 것을 확인하였다 (그림 3A, 3B). Mass Spectrometer 분석을 통해 ARD1이 Hsp70의 77번 라이신 잔기(K77)의 Acetylation을 일으키는 것을 발견하였으며 (그림 3C), 라이신(K) → 알지닌® 치환을 통해 K77R Mutant Hsp70을 제작하였을 때 스트레스에 의한 Hsp70의 Acetylation이 억제되는 것을 확인하였다 (그림 3D).
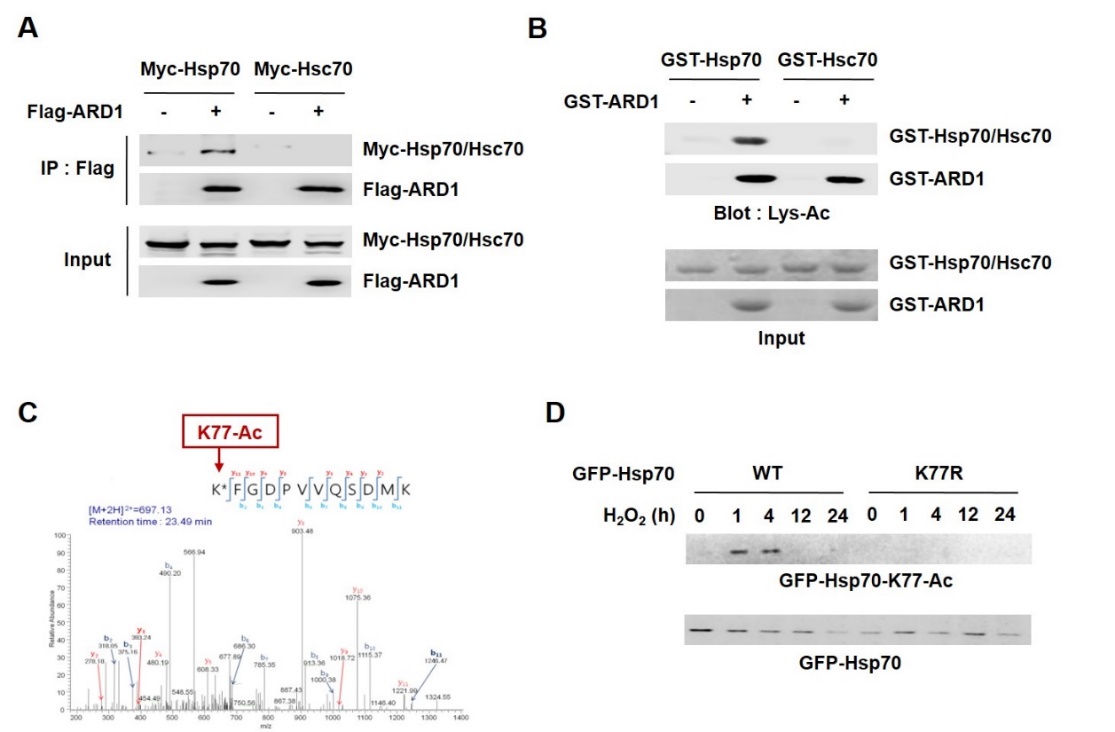
그림 3. ARD1에 의한 Hsp70의 K77잔기 Acetylation
ARD1은 Hsp70와 결합하며 (A), in vitro에서 Hsp70을 직접 Acetylation 시켰다 (B). Mass Spectrometry 분석을 통해 Hsp70의 K77 잔기가 Acetylation되는 것을 확인하였으며 (C), K77R Mutation을 통해 Hsp70의 Acetylation이 억제되는 것을 확인하였다 (D).
3. K77 Acetylation에 의한 Hsp70의 Chaperone 기능 전환 확인
K77 Acetylation이 Hsp70의 기능 전환에 미치는 영향을 알아보기 위해 Co-Chaperone 단백질과의 결합을 조사하였다. In vitro에서 Hsp70의 Acetylation이 증가할수록 Hop과의 직접적인 결합은 증가하였으며 반대로 Chip의 결합은 감소되는 것을 관찰하였다 (그림 4A). 또한 Hsp70의 Acetylation과 Deacetylation 상태를 각각 모방한 K77Q, K77R Mutant Hsp70을 사용하였을 때, 정상 Hsp70은 스트레스 초기(2시간)에 Hop과 결합하고 후기(20시간)에는 Chip과 결합하는 변화를 보이는 반면, K77R 및 K77Q Mutant Hsp70은 스트레스 상황 내내 Hop과 Chip의 결합에 변화가 없었다 (그림 4B). 이는 Hsp70의 기능이 K77 잔기의 Acetylation/Deacetylation 상태에 의존해 전환됨을 보여준다. 뿐만 아니라, 정상 Hsp70가 스트레스 후 단백질의 Refolding과 Degradation을 순차적으로 모두 수행하는 반면, K77R 및 K77Q Mutant Hsp70은 각각 Refolding 및 Degradation 기능에 결함을 보였으며 결과적으로 세포 내 단백질의 Aggregation 형성이 증가되었다 (그림 4C). 이를 통해 Acetylation/Deacetylation에 의한 Hsp70의 기능 전환이 스트레스 상황에서 세포 내 단백질의 항상성을 유지하는데 필수적인 기전임을 확인할 수 있었다.
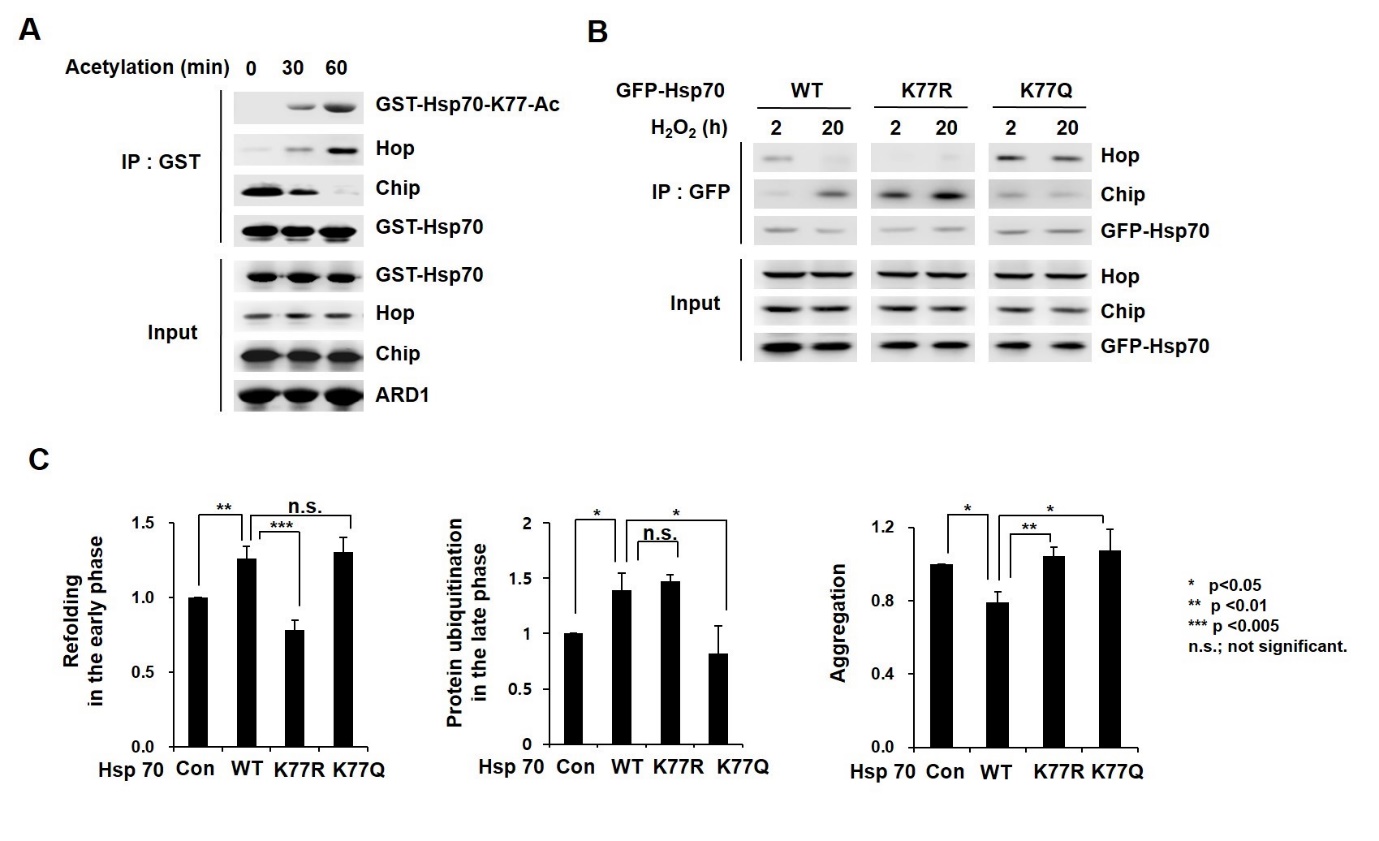
그림 4. K77 Acetylation에 의한 Hsp70의 기능 전환
In vitro에서 Hsp70의 Acetylation/Deacetylation 상태에 따라 Hop과 Chip의 결합이 결정되었다 (A). K77R 및 K77Q Mutant Hsp70을 이용하여 스트레스 초기 (2시간)와 후기 (20시간)의 Hsp70 기능이 K77의 Acetylation/Deacetylation에 의존함을 확인하였다 (B). 스트레스 상황에서 Hsp70의 기능 전환은 단백질의 Refolding/Degradation의 적절한 균형을 통해 세포 내 단백질의 항상성 유지에 기여함을 확인하였다 (C).
4. Hsp70 Acetylation의 세포 보호 효과 확인
세포 내 단백질의 항상성 유지는 결국 세포의 생존과 직결되는 부분이므로, Hsp70의 Acetylation이 스트레스 상황에서 세포의 생존에 미치는 영향을 조사하였다. 정상 Hsp70이 H2O2, Etoposide, 1-Methyl-4-Phenylpyridinium(MPP+) 와 같은 다양한 스트레스로부터 세포를 보호하는 효과를 나타내는 반면, K77R Mutant Hsp70은 세포를 보호하지 못하였다 (그림 5A, 5B). 추가적으로, 이러한 현상이 in vivo에서도 나타나는지를 확인하기 위해 Zebrafish 파킨슨병 model을 이용하였다. 정상 Hsp70과 K77R Mutant Hsp70을 발현하는 Zebrafish에 1-Methyl-4-Phenyl-1,2,3,6-Tetrahydropyridine(MPTP)를 처리하여 도파민 신경 세포의 손상을 유도하였을 때, K77R Mutant Hsp70에 의해 신경 세포의 손상이 심각해 졌으며 (그림 5C), 이에 의한 행동 장애 역시 동일한 패턴을 보였다 (그림 5D). 이러한 결과들은 Hsp70의 Acetylation이 스트레스 상황에서 세포를 보호하는데 필수적인 기전임을 보여준다.
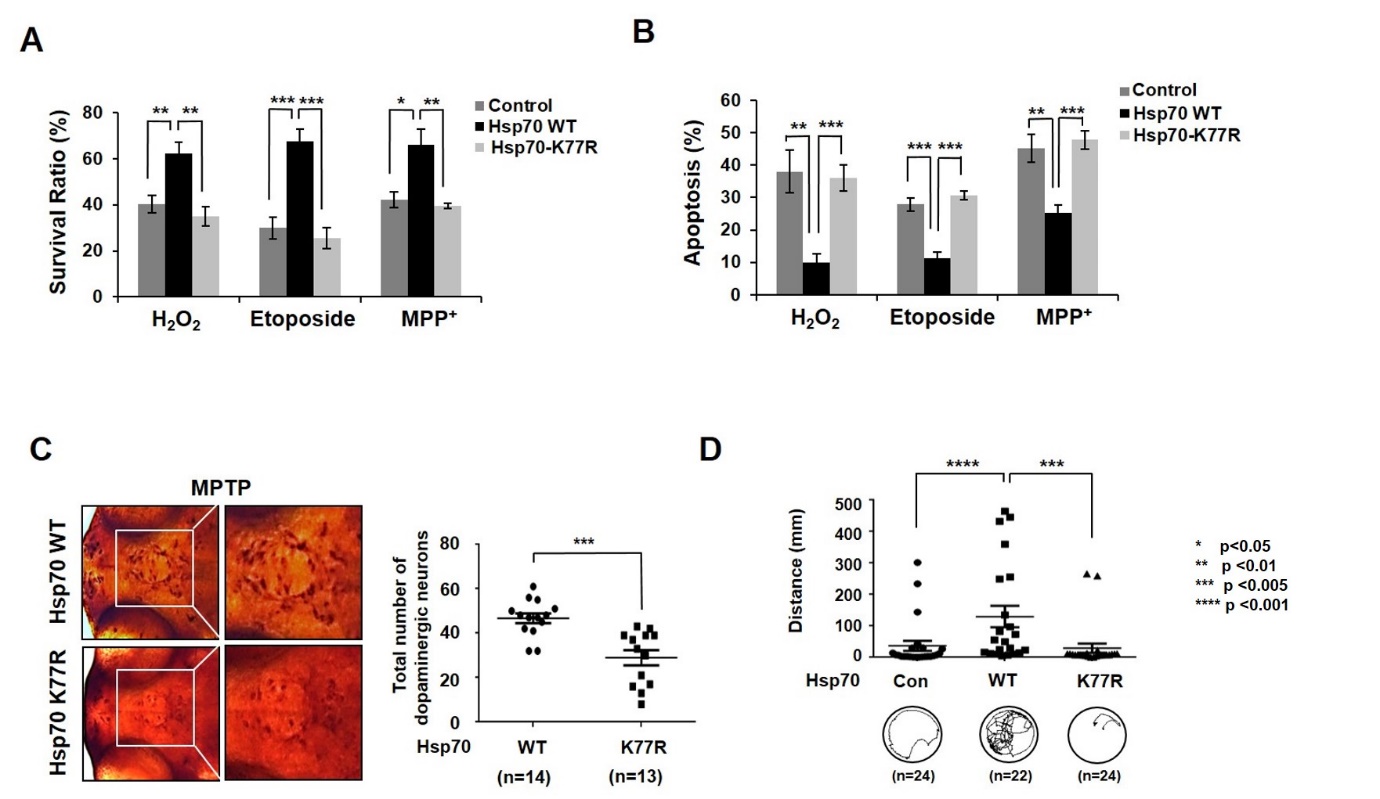
그림 5. 스트레스 상황에서 Hsp70 Acetylation에 의한 세포 보호
Hsp70 Acetylation은 다양한 스트레스 상황에서 세포 생존에 필수적이었다 (A, B). Zebrafish 파킨슨병 Model에서 도파민 신경 세포의 손상이 Hsp70 Acetylation에 의해 조절되었으며 (C), 행동 장애 역시 신경 세포 손상 정도와 비례하게 나타났다 (D).
연구의 성과 및 의의
Hsp70은 스트레스에 의해 손상된 단백질을 처리하는 기능을 수행하는데 협력하는 Co-Chaperone의 종류에 따라 수행하는 기능이 단백질 Refolding과 Degradation으로 달라진다. 본 연구에서는 Hsp70의 이 두 가지 기능이 Acetylation에 의해 조절되는 기전을 규명하였다. Hsp70은 스트레스 초기에 Acetylation되고 후기에는 다시 Deacetylation되는데, 이러한 Acetylation/Deacetylation 상태는 Hsp70이 세포 내 손상된 단백질을 복구할지 제거할지를 결정하는 일종의 스위치 역할을 한다. 스트레스 초기의 Acetylation된 Hsp70은 손상된 단백질들을 Refolding하여 우선적으로 복구하는 기능을 담당하며, 후기의 Deacetylation된 Hsp70은 복구에 실패한 단백질들을 Degradation을 통해 세포 내에서 완전히 제거해 버리는 역할을 한다. 즉, Hsp70은 Acetylation/Deacetylatoin 스위치에 의해 그 기능을 시기 적절하게 전환함으로써 세포가 스트레스에 상황에 대응하여 살아남는 것을 가능케 한다 (그림 6).
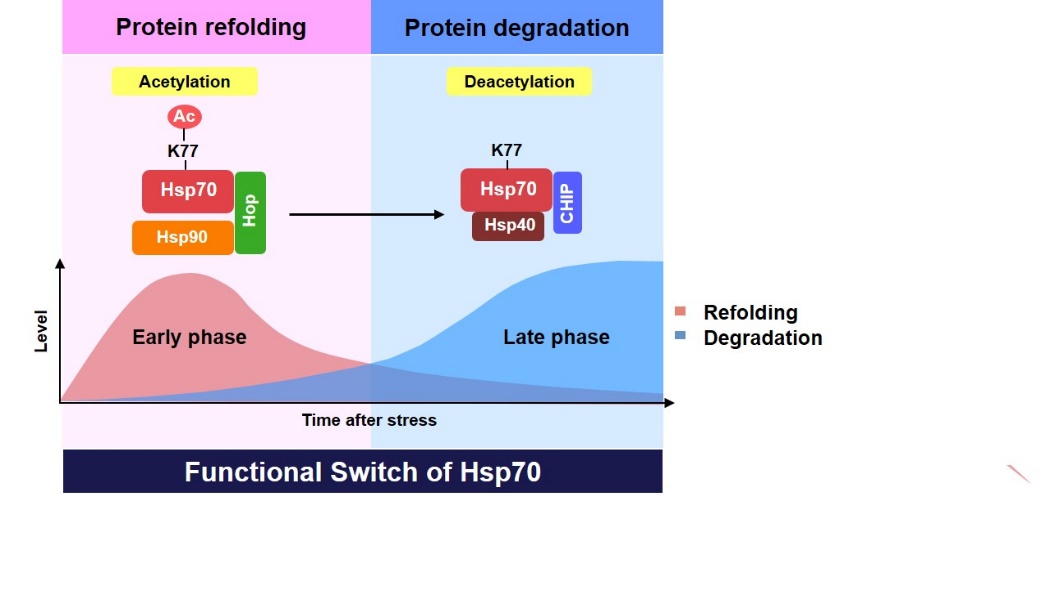
그림 6. 스트레스 상황에서 Hsp70의 기능 전환 기전
Hsp70은 스트레스 초기에 Acetylation되어 손상 단백질의 Refolding을 유도하고, 후기에는 Deacetylation 되어 Degradation을 담당한다.
본 연구를 통해 생명체가 스트레스에 대응하는 방어 기전에 대해 이해할 수 있게 되었으며, 연구 결과는 다양한 분야의 질병 치료에도 적용 가능하다. 특히, 암세포는 주변 환경에 대응하여 살아남기 위해 높은 수준의 Hsp70 발현을 유지한다고 알려져 있으므로, 본 연구 결과를 이용하여 암세포가 항암제, 방사선 치료와 같은 스트레스 상황을 극복하는 항암 내성 기전을 억제하는 방법의 개발이 가능할 것이다 (8). 뿐만 아니라, Hsp70에 의한 스트레스 방어 기전은 뇌졸중, 알츠하이머, 파킨슨병 등 다양한 중추신경계 질환에서 인체를 보호하는 작용을 한다는 것이 널리 알려져 있으므로, 본 연구 결과는 다양한 신경 질환을 예방하거나 치료할 수 있는 방법에도 폭 넓게 응용될 수 있을 것으로 기대된다 (9).
참고문헌
1. Ellis, J. (1987) Proteins as molecular chaperones. Nature 328, 378–379.
2. Ritossa, F. (1962) A new puffing pattern induced by temperature shock and DNP in drosophila.
Cell Mol Life Sci 18, 571-573
3. Hartl, F. U., Bracher, A. and Hayer-Hartl, M. Molecular chaperones in protein folding and proteostasis.
Nature 475, 324–332 (2011).
4. Hohfeld, J., Cyr, D. M. and Patterson, C. (2001) From the cradle to the grave: molecular chaperones that may
choose between folding and degradation. EMBO Rep 2, 885–890.
5. Cho, H. S., Shimazu, T., Toyokawa, G. et al. (2012). Enhanced HSP70 lysine methylation promotes proliferation of
cancer cells through activation of Aurora kinase B. Nat Commun 3, 1072.
6. Truman, A. W., Kristjansdottir, K., Wolfgeher, D. et al. (2012) CDK-dependent Hsp70 phosphorylation controls
G1cyclin abundance and cell-cycle progression. Cell 151, 1308–1318.
7. Yang, Y. Fiskus, W., Yong, B. et al. (2013) Acetylated hsp70 and KAP1-mediated Vps34 SUMOylation is required for
autophagosome creation in autophagy. Proc Natl Acad Sci USA 110, 6841-6846.
8. Murphy, M. E. (2013) The HSP70 family and cancer. Carcinogenesis 34, 1181–1188.
9. Morimoto, R. I. and Santoro, M. G. (1998) Stress-inducible responses and heat shock proteins: new pharmacologic
targets for cytoprotection. Nat Biotechnol 16, 833–838.
첨부파일