
생화학분자생물학회입니다.
Laboratory of Molecular Regenerative Medicine
작성자
관리자작성일자
2016-09-01조회수
352Laboratory of Molecular Regenerative Medicine
김진홍
서울대학교 자연과학대학 생명과학부
[연구실소개]
본 연구실에서는 분자생물학적 연구를 통해 질병 조직의 재생신호전달 체계를 규명하고 이를 적용해 조직재생을 통한 근본적인 질병치료를 목표로 하는 연구를 수행하고 있다. 포유동물의 신생개체는 높은 재생능력을 보이지만 성체가 됨에 따라 생체 재생능력을 점차적으로 잃어버리게 되어 노화 및 외상 등의 다양한 요인에 의해 조직의 기능이 손실된다. 우리는 이러한 성체조직에 내재되어있는 재생(Regeneration)의 신호전달체계를 규명하고 이를 활용해 개체 수준에서의 재생능력을 향상시키는 치료전략까지 개발하고자 한다. 특히, 노화, 외상 등의 퇴행성 변화에 의해 유발되는 근골격계 퇴행성질환의 재생치료에 관한 연구를 중점적으로 진행하고 있다.
퇴행성 관절염, 난치성 오십견 등으로 대표되는 근골격계 퇴행성질환은 증가하는 고령화 추세와 함께 많은 환자들의 삶의 질을 떨어뜨리고 있다. 하지만 근골격계 퇴행성질환의 치료는 단순히 통증 완화를 위한 약물 치료 및 외과적 수술에 초점을 두고 있어 퇴행 조직의 근본적인 치료법을 제시하지 못하는 실정이다. 본 연구실에서는 이러한 근골격계 퇴행성 조직의 재생 신호전달체계를 규명하고 이를 적용하여 근본적인 재생치료를 목표로 한다. 이러한 목표로 분자수준에서의 연구에서부터 다양한 질병 동물 모델 및 퇴행성질환 환자 샘플을 이용한 실질적 개체수준의 분석까지 다각적 측면으로 질병의 병리기전을 이해하고 이것을 기반으로 근골격계 퇴행성질환의 근본적인 조직재생을 유도하여 실질적으로 질병치료가 가능한 재생치료제 개발연구를 수행하고 있다.
1. 근골격계 퇴행조직의 재생을 유도하는 재생유도인자 발굴
근골격계 조직은 다량의 Extracellular Matrix(ECM)로 이루어져 있으며 이러한 ECM의 Anabolism과 Catabolism이 적절한 균형을 이루어 항상성을 유지하고(Fig. 1) 이는 조직의 구조적 지지, 완충작용 등 조직기능에 중요한 역할을 한다. 정상적인 조직은 이러한 항상성이 유지되어 적절한 기능을 하지만 퇴행이 유도된 근골격계 조직은 Anabolism과 Catabolism의 불균형으로 ECM의 감소가 유발되고 정상적인 기능을 하지 못하게 된다. 이러한 이유로 근골격계 퇴행성질환 환자들은 운동의 불편에서부터 그 정도에 따라 심각한 통증까지 겪게 된다.
이러한 ECM의 항상성 조절의 측면에서 Anabolism Mechanism을 조절하는 핵심 Molecule을 밝혀냄으로써 근골격계 조직재생 유도인자를 발굴하고자 한다. Proteomics를 통해 ECM 합성을 조절하는 핵심 전사인자의 새로운 Modification을 분석하여 전사활성을 증가시키는 Post-Transcriptional Modification(PTM) Mechanism을 연구하고 있다. 이러한 PTM을 조절하는 상위 단백질의 기능을 저해시킴으로써 ECM합성이 증대되며 생체 내에서 근골격계 퇴행성질환의 완화 효과를 관측하고 있다. 또 다른 재생유도인자 발굴을 위해 miRNA에 의한 ECM합성 인자들의 후성적 조절에 관한 연구도 진행 중에 있다.
이러한 방향으로 새롭게 발굴한 재생유도인자의 조절을 통하여 세포 내 내재된 재생시스템을 활성을 조절하는 새로운 재생치료제 개발의 초석으로 사용하고 있다.
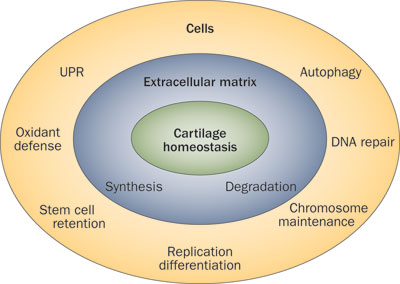
Figure. 1 Cartilage Homeostasis (Martin K. Lotz, Beatriz Caramés. Nat. Rev. Rheumatol. 2011)
2. Small Molecule, Genetic Module, Stem Cell Therapy
본 연구실은 근골격계 조직의 재생유도유전자의 발굴에서 그치는 것이 아니라 재생유도인자의 조절을 통해 조직재생을 유도하고자 Small Molecule, Genetic Module, Stem Cell Therapy등을 이용한 재생치료제를 개발하고 있다.
Small Molecule은 적은 분자량을 가진 Organic Compound로 조직 내 투과가 용이하고 세포 내의 생물학적 Process 조절이 가능하다는 장점을 가지고 있다. 우리는 이러한 Small Molecule을 이용해 재생유도인자를 조절하는데 이용한다. 재생유도인자의 조절을 통해 손상된 근골격계 조직의 재생을 유도하는 효과를 검증하는 연구를 수행 중에 있다.
또한, Stem Cell Therapy를 이용한 조직재생치료 연구 또한 진행 중에 있다. Stem Cell Therapy를 위해서는 줄기세포의 올바른 조직세포로의 분화가 가능한 제어기술이 필요하다. 이를 위해 적절한 조직세포로 분화를 유도할 수 있는 ‘분화유도유전자’를 발굴하고, 분화유도유전자의 발현을 적절한 시기에서 조절하는 System인 ‘Genetic Module’을 탑재한 줄기세포치료제를 개발하는 것을 목표로 하고 있다. 이러한 줄기세포치료제는 근골격계 조직으로의 분화를 유도하는 유전자를 통해 적절한 분화를 촉진할 수 있다. 또한 근골격계 조직세포로의 분화가 유도된 이후에는 분화유도유전자의 발현을 억제하는 Genetic Module 시스템을 갖고 있어 지속적인 분화, 분열에 의한 부작용을 최소화하여 효과적인 재생치료제로서의 기능을 할 것으로 기대한다(Fig. 2).
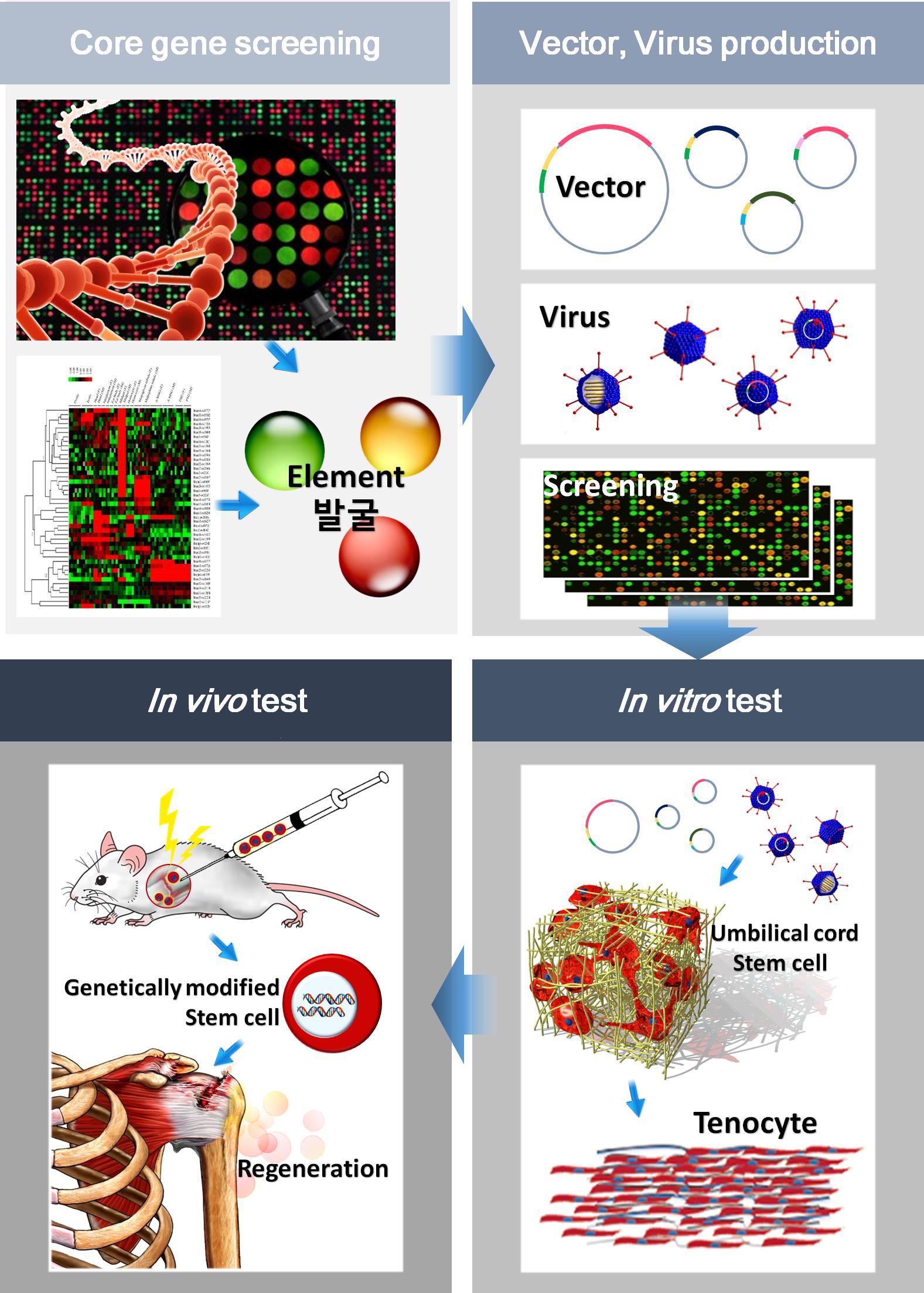
Figure 2. Overview of Stem Cell Therapy
3. 근골격계 재생치료로의 적용
본 연구실이 발굴한 재생유도인자와 이를 조절할 수 있는 Small Molecule, 재생유도인자를 이용한 Stem Cell Therapy는 근·골격계의 재생을 유도하여 노년층에서 흔히 발생하는 퇴행성관절염 및 난치성오십견의 새로운 치료전략을 수립하고 있다. 해당 질병에 대한 실질적인 효과는 본 연구진이 보유하고 있는 내측반월판 절개술(DMM)을 통한 퇴행성관절염 모델 마우스와 극상근 절제술을 통한 난치성오십견 모델 마우스를 이용하여 동물모델 개체수준에서 확인하고 있다. 또한, Hydrogel Injection기법을 이용한 Small Molecule의 Controlled Release로 해당 조직에 지속적인 전달을 통하여 재생치료제의 효능을 극대화하는 연구를 수행하고 있다.
[연구책임자]

김진홍 교수
주소: 서울특별시 관악구 관악로 1 서울대학교 자연과학대학 생명과학부
전화: 02-880-4178
E-mail: jinhkim@snu.ac.kr
Homepage: http://biosci.snu.ac.kr/jinhkim
[연구진구성]
교수: 김진홍
박사과정: 김현섭
석박통합과정: 조용식, 김현경, 강동현, 신중권
석사과정: 천동현, 김수경
연구원: 구영란

[대표논문]
1. Won, Y., Shin, Y., Chun, C.H., Cho, Y., Ha, C., Kim, J.H. and Chun, J.S. (2016) Pleiotropic roles of
metallothioneins as regulators of chondrocyte apoptosis and catabolic and anabolic pathways during osteoarthritis
pathogenesis. Annals of the Rheumatic Diseases. E-pub ahead of print.
2. Lee, M., Won, Y., Shin, Y., Kim, J.H. and Chun, J.S. (2015) Reciprocal activation of hypoxia-inducible factor
(HIF)-2 and the zinc-ZIP8-MTF1 axis amplifies catabolic signaling in osteoarthritis.
Osteoarthritis and Cartilage 24(1):134-45.
3. Kim, H., Kang, D., Cho, Y. and Kim, J.H. (2015) Epigenetic regulation of chondrocyte catabolism and anabolism
in osteoarthritis. Mol. Cells 38(8): 677-684.
4. Kim, J.H., Lee, G., Won, Y., Lee, M., Kwak, J.S., Chun, C.H., Chun, J.S. (2015) Matrix crosslinking-mediated
mechanotransduction promotes post-traumatic osteoarthritis. Proc. Natl. Acad. Sci. USA 112(30):9424-9.
5. Kim, J.H., Jeon, J., Shin, M., Won, Y., Lee, M., Kwak, J.S., Lee, G., Rhee, J., Ryu, J.H., Chun, C.H.,
Chun, J.S. (2014) Regulation of the catabolic cascade in osteoarthritis by the zinc•ZIP8•MTF1 axis.
Cell 156(4): 730-743
6. Kim, J.H. and Asthagiri, A.R. (2011) Matrix stiffening sensitizes epithelial cells to EGF and enables the
loss of contact inhibition of proliferation. Journal of Cell Science 124(Pt 8):1280-7.
7. Kim, J.H., Dooling, L., Asthagiri. AR. (2010) Intercellular mechanotransduction during multicellular
morphodynamics. Journal of Royal Society Interface 7, S341–S350.
8. Kim, J.H., Kushiro, K., Graham, N.A., Asthagiri, A.R. (2009) Tunable interplay between epidermal growth factor
and cell-cell contact governs the spatial dynamics of epithelial growth.
Proc. Natl. Acad. Sci. USA 106(27):11149-53.