
생화학분자생물학회입니다.
유전체 및 중개의학연구실
작성자
관리자작성일자
2015-12-01조회수
759가천대학교 의과대학 유전체 및 중개의학연구실 (舊, 분자내분비연구실)
이시훈
가천대학교 의과대학 내과학교실, 유전체 및 중개의학연구실
[연구실 소개]
연혁
2008년 3월 이시훈 교수가 미국 국립보건원(NIH)에서 박사 후 과정 연수를 마치고 가천의대로 부임하면서 ‘분자내분비연구실’이라는 명칭으로 연구실을 개설하였다. 기초 연구를 위한 실험실은 인천광역시 송도 신도시에 최첨단 시설로 개소된 가천의대 이길여암당뇨연구원에 개설되었고, 환자 진료 및 임상 시험은 구월동에 위치한 가천대 길병원에서 진행되었다. 개설 당시 연구비 재원은 당시 한국과학재단(現 연구재단)의 신진연구자 지원사업과 생명보험사회공헌재단의 희귀난치질환 극복 연구비 지원사업, 그리고 대한당뇨병학회, 대한내분비학회의 우수연구자 지원사업 그리고 가천대 길병원 원내 연구비 지원 사업으로 조성되었다. 주로 진료실에서 발견된 흥미롭고 연구의 진행 가치가 있을 것으로 판단되는 환자 및 그 가족 구성원들을 대상으로 임상적 정보와 더불어 유전학적인 배경을 규명하는 연구를 진행하였으며, 새롭게 알려진 결과를 바탕으로 해당 환자 및 가족뿐만 아니라 관련이 있는 다른 다수의 환자군에게 적용될 수 있는 임상적 응용 및 중개의학으로의 이행을 목적으로 연구를 진행 중으로 오늘날에 이르고 있다.
모토
진료실에서 발견된 흥미롭고 해결되지 않은 임상적 의문들을 각종 분자 및 세포유전학적 연구 방법을 동원하여 그 원인 및 진행과정을 규명하고, 실험실에서 도출된 새롭고 놀라운 사실들을 환자의 진단, 치료, 예후의 평가 및 예방적 목적을 위해 적용하는 중개의학의 원활하고 효율적인 쌍방향 소통을 위한 연구의 진행 및 이를 위해 가장 적절하게 훈련된 연구자의 육성을 우리 연구실의 목표로 한다.
[연구성과]
1. Experimental PTH Gene Therapy Using Phi C31 Integrase
표적 특이적인 유전자 도입을 가능하게 하는 Phi C31 Integrase를 이용하여 (그림 1) 부갑상선 호르몬(PTH) 유전자의 실험적 유전자 치료를 시도하였고, 세포 내 실험과 실험 동물에서 효과적인 PTH 분비를 확인하였다. 칼슘 농도에 따른 PTH 분비 조절 능력이 부족한 한계점 때문에 영향력 높은 논문에 게재하지 못하였으나 PTH를 대상으로 한 유전자 치료의 첫 번째 시도로 인정받았다. 추후 칼슘 농도에 따른 PTH 분비를 조절할 수 있는 CaSR의 기능을 추가한다면 임상적으로 실현 가능성을 높일 수 있을 것으로 기대하고 있으며, 이를 위해 PTH 분비 세포의 제작을 위해 여러 가지 접근을 시도 중에 있다.
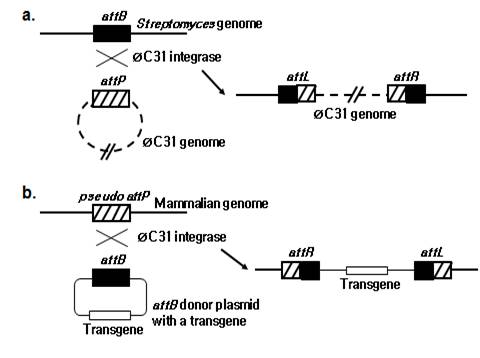
그림 1. Phi C31 Integrase를 이용한 유전자 도입과 응용
2. Korean Hypopara Registry Study
국내 특발성 부갑상선 기능저하증 환자의 실태를 조사하기 위하여 전국적으로 환자 등록 사업을 시행 중으로 현재 약 30 여 건 이상의 증례를 등록하였다.
이 환자들을 대상으로 pre-pro-PTH, GCM2, CaSR, GATA3의 염기 서열을 분석하였고, 이 중 가족력이 있는 네 가계에서는 Whole-Exome Sequencing을 시행하였으며 각각 GCM2 C106R, CaSR D410E, CaSR P221L, PTH R25C 돌연변이를 발견하였다. 이 중 이미 보고된 CaSR P221L을 제외한 나머지 돌연변이들은 아직 보고가 되지 않은 새로운 돌연변이로써, 각 유전자의 돌연변이의 기능성 평가를 통해 질병 원인 유전자 돌연변이임을 규명하는 연구가 진행되었다.
3. GCM2 C106R
특발성 부갑상선 기능저하증에 이환된 모자에서 부갑상선 특이 전사제어인자인 GCM2 C106R 돌 연변이를 발견하였고 기능성 평가를 통해 원인 유전자 돌연변이임을 규명하였다 (그림 2).
GCM(Glial Cell Missing) 유전자는 당초 초파리에서 Glial Cell의 분화에 중요한 역할을 하는 것으로 알려졌고 고등 포유류(쥐, 사람)에서는 GCM1, GCM2의 두 가지 아형이 존재하며 이는 현재 이화여대에 재직 중인 김재상 교수님에 의해 처음 발견되었다. 신경계에서 중요한 역할을 할 것으로 예상했던 기대와는 다르게 GCM1은 임신 시 태반에, GCM2는 부갑상선에만 발현이 국한된 것으로 밝혀졌으며 GCM2의 기능을 소실시킨 쥐에서 부갑상선이 전혀 생성되지 않는 사실로 이는 부갑상선의 발생 과정에 매우 중요한 역할을 하는 전사제어인자로 생각되었다. 이 후 특발성 부갑상선 기능저하증 가계에서 몇 건의 돌연변이가 보고되었다.
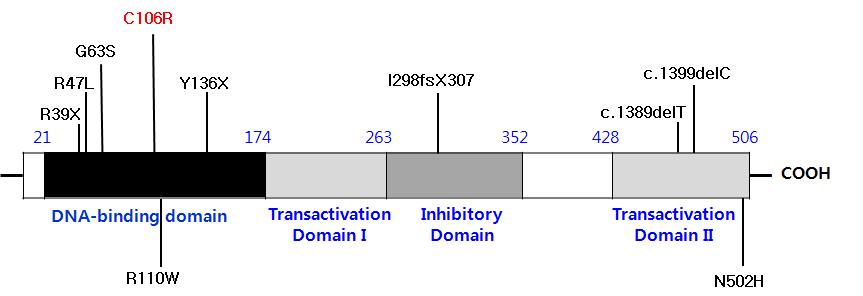
현재까지 규명된 GCM2의 돌연변이는 10개 이내로 DNA Binding Domain에 발생한 Autosomal Recessive 유전 양식의 Homozygous Mutation과 Carboxy Terminal의 TA Domain에 발생한 Autosomal Dominant 유전 양식의 Heterozygous Mutation으로 대별할 수 있는데 (그림 3), 본 연구실에서 발견한 C106R Mutation은 DNA Binding Domain에 존재하는 Heterozygous Mutation으로써 기능 평가상 Autosomal Recessive 유전 양식을 보이나 실제 환자에서는 Autosomal Dominant 유전 양식을 보여 일치하지 않음을 보여 이에 규명하기 위한 추가 연구가 필요하다. GCM2는 부갑상선 형성 과정에서 매우 중요한 전사제어인자인 동시에 태생 이후 성체에서도 지속적으로 발현이 꾸준하게 증가해 있는 사실로 미루어 발생기의 기능과는 다른 중요한 기능을 담당하고 있을 것으로 사료되어 이의 표적 유전자를 규명하고 기능을 규명하는 연구가 진행 중에 있다.
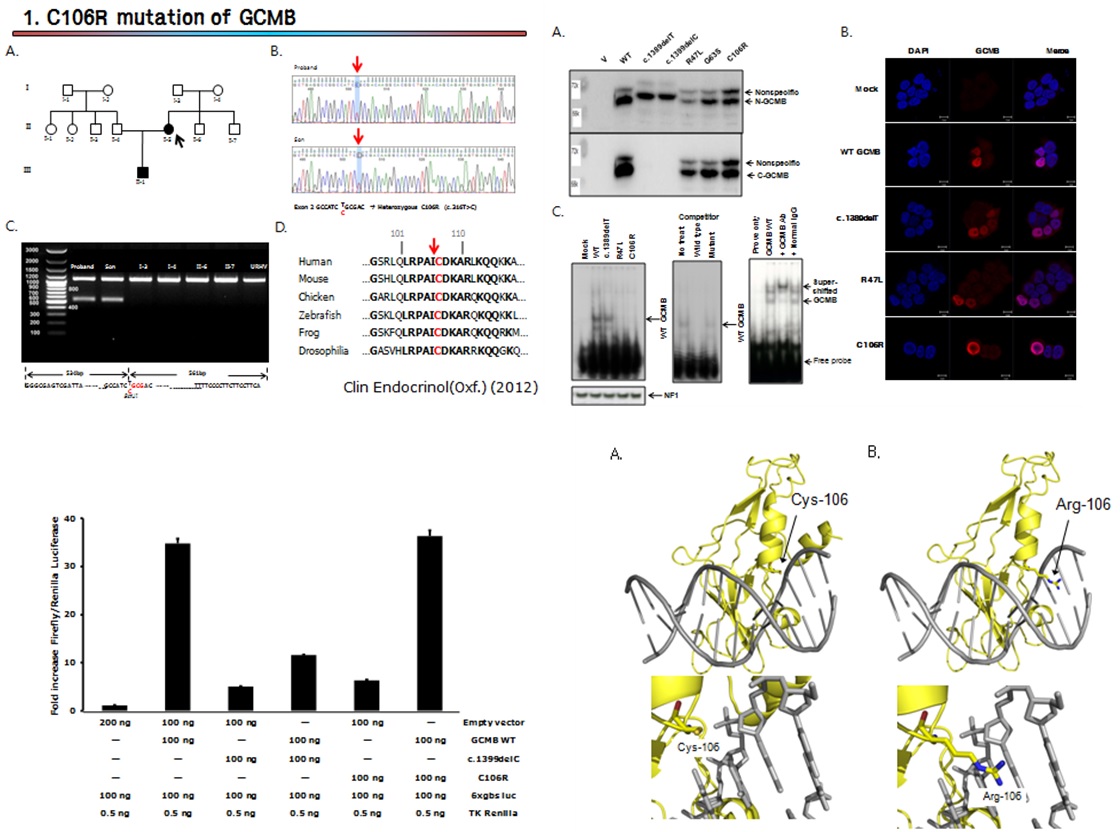
그림 2. GCM2 C106R 돌연변이와 기능성 평가
4. CaSR D410E
특발성 부갑상선 기능저하증에 이환된 모녀에서 CaSR D410E의 돌연변이를 발견하였고 기능평가를 통해 원인 유전자의 돌연변이임을 확인하였다 (그림 4). CaSR은 약제 개발의 표적이 되는 매우 유망한 GPCR 중 하나이며 효현제(Calcimimetics)의 경우, 일차성, 이차성 부갑상선 기능항진증에 효과적인 약제로 이미 개발이 되어 있고 길항제(Calcilytics)는 체내 부갑상선 호르몬의 분비를 자극하여 효과적인 골다공증 치료제로 개발 중인데 아직까지 확실한 골형성의 촉진에 의한 골밀도의 증가를 입증한 약제를 보고되지 않은 실정이다. 우리 연구실에서는 새롭게 개발 중인 한 Calcilytics의 가족성 저칼슘혈증의 치료제로서의 가능성을 최초로 실험적으로 규명하였으며 차후 임상 시험을 통해 임상적 가치를 규명할 예정이다.
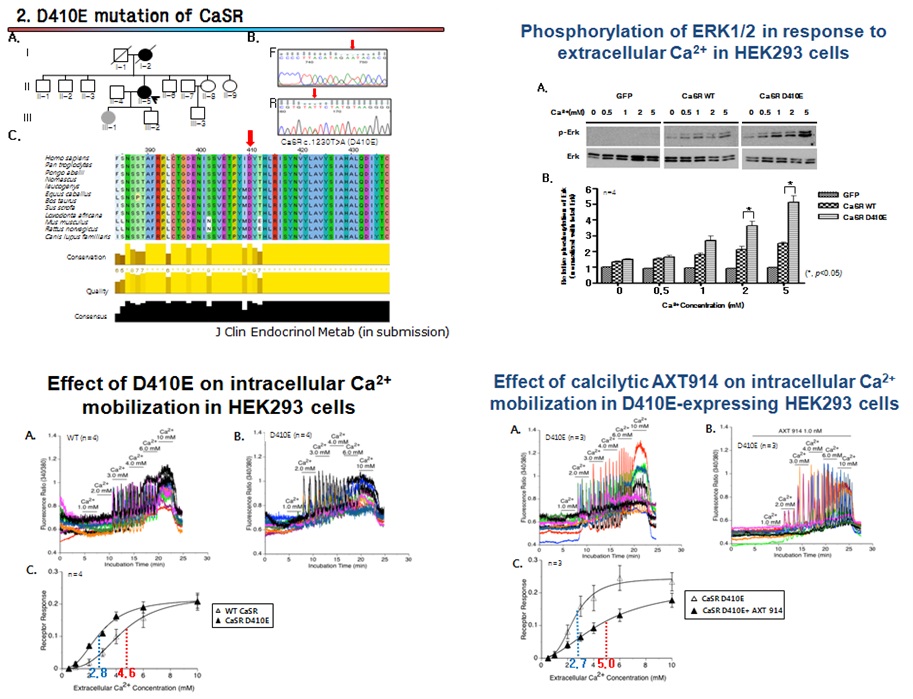
그림 4. CaSR D410E 돌연변이와 기능성 평가
[진행 연구 및 계획]
1. PTH R25C
본 연구실에서는 최근에 한 특발성 부갑상선 기능저하증 가계에서 PTH R25C 돌연변이를 발견하였으며 각종 기능연구를 통해 발병 원인 유전자 변이임을 규명하였다. 이는 PTH Encoding Gene에서 발견된 최초의 돌연변이이며 이를 통하여 PTH와 PTHR1과의 상호 관계 및 GPCR을 경유하는 세포 내 신호 전달 체계에 대한 새로운 사실들, 그리고 이를 임상적으로 응용할 수 있는 광범위하고 깊은 수준의 연구를 계획하고 진행 중에 있다.
본 연구실에서 갑상선 제2형 탈요오드화효소(Deiodinase Type 2, DIO2)의 기능 저하와 관련된 새로운 형태의 유전적 변이를 찾아 이를 기능연구를 통해 규명하였고, 이는 SBP2 유전자 변이에 이은 두 번째 변이로 생각하고 있다. 이를 확대, 심화하여 DIO2의 기능을 조절하는 기전을 밝히고 효과적으로 세포, 조직, 장기 특이적인 탈요오드화효소의 활성을 통해 특정 임상 효과를 이용하면 획기적인 약제 개발이 가능할 것으로 기대하고 있다.
3. Undiagnosed Patients Program
실제 임상 현장에서 맞닥뜨리게 되는 임상적으로 해결되지 않은 수 많은 임상례들을 선별하여 전장 유전체 분석을 통해 원인 유전체 변이를 발굴하고, 관련된 새로운 (병태)생리에 대한 이해를 깊게 하여 해당 질환뿐만 아니라 연관된 더욱 흔한 질환의 치료법 및 예방법을 개발하는 것이 본 연구실의 궁극적 계획이자 목표이다.
4. 임상 시험
현재 Sclerostin 항체를 이용한 골다공증의 치료제인 Romosozumab의 국제 다기관 공동 임상연구 이외에 각종 당뇨병 신약에 대한 임상연구를 진행 중이며, 부갑상선 기능저하증 환자를 대상으로 부갑상선 호르몬 보충 요법에 대한 임상 시험을 계획 중에 있다. 이 외에도 임상 전시험과 초기 임상을 비롯한 다양한 심층 임상연구를 시행할 계획이다.
[연구책임자]
|
|
성명: 이시훈 주소: 인천광역시 남동구 구월동 1198 가천대 길병원 내분비대사내과 전화: 032-460-8207 Email: shleemd@gachon.ac.kr |
[연구진 구성]

<유전체 및 중개의학연구실 현 연구실원>

<유전체 및 중개의학연구실 현 연구실원 및 졸업생>
이시훈 교수, 안현정 박사, 정상원 대학원생, 지은현 대학원생, 이선화 연구간호사 이현승 박사, 최홍석 공보의, 강현정 비서
[대표논문]
| 1. | Muniyappa R, Lee S, Chen H, Quon MJ. (2008) Current Approaches for Assessing Insulin Sensitivity and Resistance In Vivo: advantages, limitations, and appropriate usage. Am J Physiol Endocrinol Metab 294:E15-E26 |
| 2. | Lee S, Muniyappa R, Yan X, Chen H, Yue LQ, Hong E-G, Kim JK, Quon MJ. (2008) Comparison Between Surrogate Indexes of Insulin Sensitivity/Resistance and Hyperinsulinemic Euglycemic Glucose Clamp Estimates in Mice. Am J Physiol Endocrinol Metab 294:E261-E270 |
| 3. | Lee S, Lynn EG, Kim J-a, Quon MJ. (2008) Protein Kinase C-ζ phosphorylates Insulin Receptor Substrate-1, -3, and -4, but not -2: isoform specific determinants of specificity in insulin signaling. Endocrinology 149:2451-2458 |
| 4. | Lee S, Hong SW, Choi HS, Lee LY, Nam C, Rhee Y, Chung U-i, Lim S-K. (2008) Experimental Parathyroid Hormone Gene Therapy using Phi C31 Integrase. Endocrine J 55:1033-1041 |
| 5. | Lee S, Ha M, Eom YS, Ie Park IB. (2009) Role of Unilateral Aderenalectomy in ACTH-Independent Macronodular Adrenal Hyperplasia. World J Surg 33:157-158 |
| 6. | Yi HS, Choi B, Lee S. (2011) Molecular understanding and assessment of hypoparathyroidism. Endocrinol Metab (Seoul) 26:25-32 |
| 7. | Yi HS, Kim SH, Kim J, Bae EJ, Hong S, Park IB, Lee S. (2011) Mutational Analysis of the NF-1 Gene in Two Families with Neurofibromatosis 1 accompanied by Pheochromocytoma. Endocrinol Metab (Seoul) 26:177-184 |
| 8. | Yi HS, Eom YS, Park IB, Lee S, Hong S, Jueppner H, Mannstadt M, Lee S. (2012) Identification and characterization of C106R, a novel mutation in the DNA-binding domain of GCMB, in a family with autosomal dominant hypoparathyroidism. Clin Endocrinol (Oxf) 76:625-633 |
| 9. | Nam H-J, Jung IH, Kim J, Kim JH, Suh J, Kim HS, Kim HK, Jung YJ, Kang JW, Lee S. (2012) Association between brachial-ankle pulse wave velocity and occult coronary artery disease detected by multi-detector computed tomography. Int J Cardiol 157:227-232 |
| 10. | Park SY, Mun H-C, Eom YS, Baek HL, Jung TS, Kim CH, Hong S, Lee S. (2013) Identification and characterization of D410E, a novel mutation in the loop 3 domain of CaSR, in autosomal dominant hypocalcemia and a therapeutic approach using a novel calcilytic, AXT914. Clin Endocrinol (Oxf.) 78:687-693 |
| 11. | Park SY, Eom YS, Choi B, Yi HS, Yu S-H, Lee K, Jin H-S, Chung Y-S, Jung TS, Lee S. (2013) Genetic and Clinical Characteristics of Korean Patients with Isolated Hypoparathyroidism: From the Korean Hypopara Registry Study. J Korean Med Sci. 28:1489-1495 |
| 12. | Lee DM, Yu S-H, Yoon HH, Lee KL, Eom YS, Lee K, Kim BJ, Kim YS, Park IB, Kim KW, Lee S. (2014)Genetic Analysis of MEN1 Could Lead to Misdiagnosis of an Extremely Rare Presentation of Intrasellar Cavernous Hemangioma as MEN1. Endocrinol Metab. (Seoul) 29:146-153 |
| 13. | Lee S, Mannstadt M, Guo J, Kim SM, Yi H-S, Khatri A, Dean T, Okazaki M, Gardella TJ, Jueppner H. (2015) A Homozygous [Cys25]PTH(1_84) Mutation that Impairs PTH/PTHrP Receptor Activation Defines a Novel form of Hypoparathyroidism. J Bone Miner Res 30:1803-1813 |