
생화학분자생물학회입니다.
Laboratory of Cancer Metabolism and Metabolic Toxicity
작성자
관리자작성일자
2020-03-09조회수
710Laboratory of Cancer Metabolism and Metabolic Toxicity
Department of Molecular, Cell and Cancer Biology
University of Massachusetts Medical School
Lab summary
본 연구실은 한 명의 postdoc과 4명의 학생으로 구성되어 있으며, 암 특이적으로 일어나는 metabolic pathway 의 변화를 이해하고, 그 변화를 치료목적으로 활용하는 연구를 수행하고 있다. 최근 연구를 통해 암세포 특이적으로 발생되는 inherently toxic한 metabolite를 발견하였고, 이 metabolite를 해독하는 효소를 억제함으로서, 축적된 toxic metabolite가 암세포를 사멸한다는 결과를 얻었다. 또한 본 연구실은 암 이외의 다양한 질병에서 일어나는 metabolic pathway변화를 이해하고 이와 관련된 toxic metabolite의 역할 규명 및 기전 연구도 동시에 수행하고 있다.
Research Areas
1. ‘endotoxome’의 정의
본 연구실은 metabolic intermediate가 inherently toxic하다는 개념을 바탕으로, 항암 물질이나 질병의 원인 물질로서의 toxic metabolite의 역할을 탐구하기 위한 체계적 플랫폼을 구축하였다. 인간 게놈은 1,872개의 대사 효소를 발현하는데, 각각의 substrate와 product, 그리고 TOXNET(toxnet.nlm.nih.gov)과 Toxin, Target Database (http://www.t3db.ca)를 포함한 일련의 독성/화학 안전 데이터베이스를 상호 참조하여 약 200개의독성을 가진metabolic intermediate 을 목록화 하여 "endotoxome"이라고 정의 하였다 (Figure 1). 이러한 독성 대사물은 크게 다섯 가지 범주로 분류되는데 1) 반응성 aldehyde와 quinine과 같은 반응성 그룹을 가진 대사물, 2) prooxidants, 3) excitotoxin/receptor agonists, 4) 정상 대사물의 substrate analogue, 5) 메커니즘을 알 수 없는 독성 대사물들 로 나뉘어 진다. 이런toxic intermediate을 분해/대사 하여 독성을 없애는 세포내 효소들을 'detoxifiers' 로 정의하며, 이 detoxifier 가 손실이 되면 세포내 toxic intermediate이 축적되어 세포 사멸을 유도하게 된다. 본 연구실은 새로운 toxic intermediate과 이것을 대사하는 효소 (detoxifier)를 찾고 그 조절 기전을 연구하여, 새로운 metabolic pathway와 다양한 질병과의 연관성을 밝히는데 집중하고 있다.
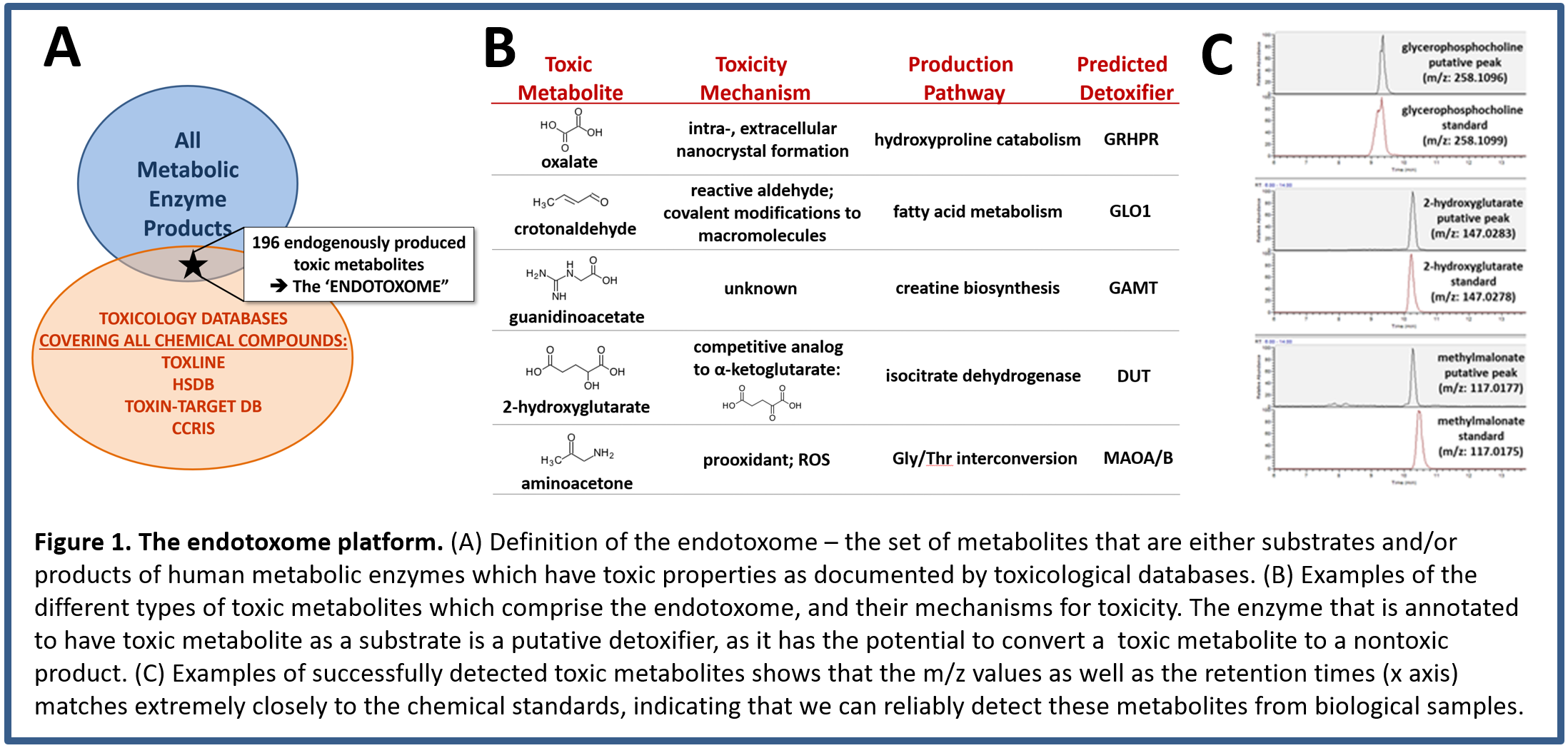
2. Detoxifying enzymes as targets for cancer therapy
흔히 이런 toxic metabolite는 효소 1에서 합성이 되며 효소 2는 이런 toxic metabolite를 분해하여 그 독성을 제거하게 되는데, detoxifier 인 효소 2를 제거하게 되면 세포 내 축적된 toxic metabolite는 세포 사멸을 유도하게 된다 (kitchen sink 개념, 그림 2). 따라서, 본 연구실은 genome-wide CRISPR/Cas9 스크리닝 시스템을 사용하여 다양한 암세포에서 암세포 특이적으로 발생하는 toxic metabolite를 제거하는detoxifier를 발굴하고 조절 기전을 규명하는 연구를 통해 metabolic pathway 조절을 통한 암 치료에 사용하려고 한다. 또한 특정 암세포에서 과활성화된 metabolic pathway 연구를 통해 선택적으로 축적된 metabolite를 예측하고 항암 치료에 사용하려고 한다.
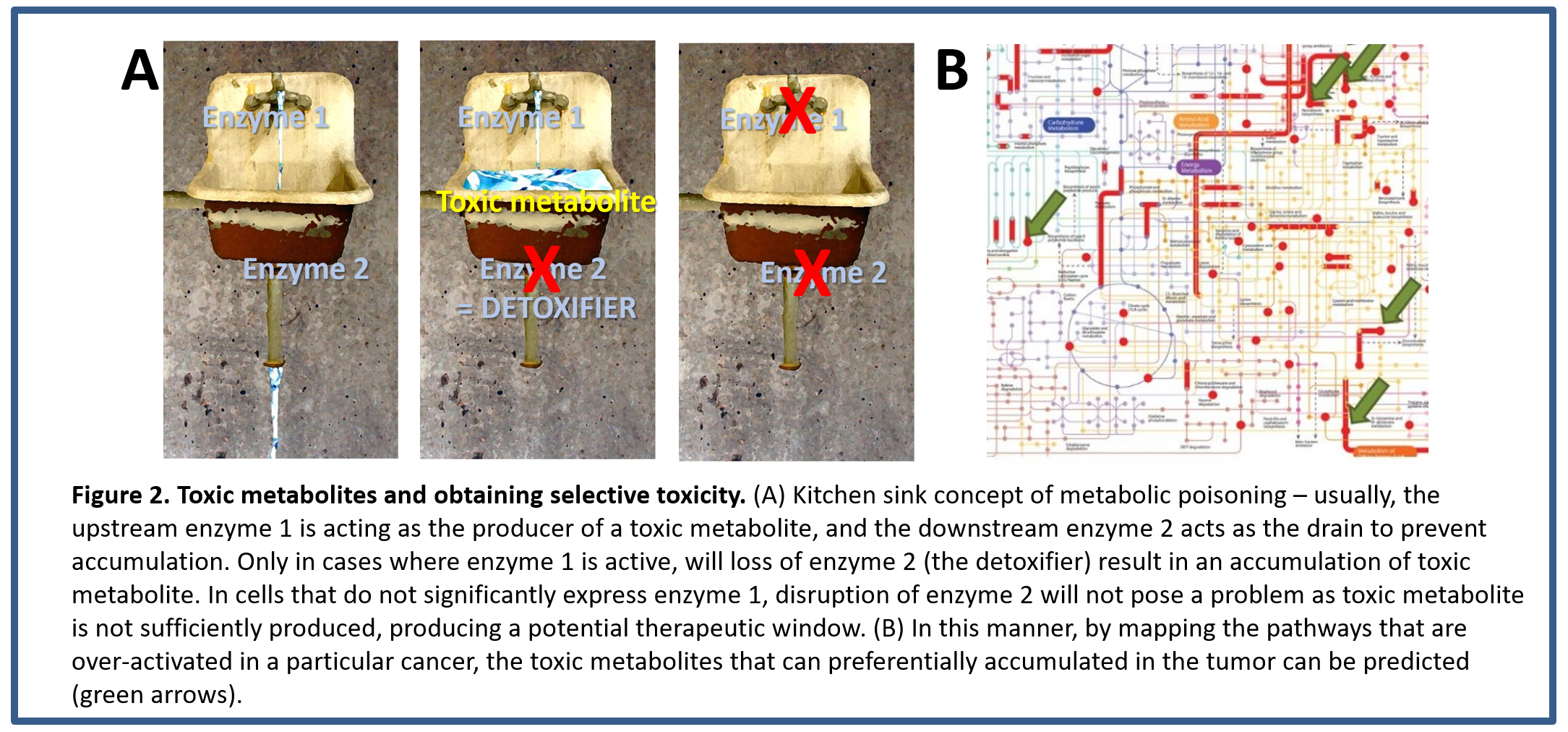
3. Understanding the role of GCAT and -to- conversion in physiology and in cancer 후생생물에서Glycine C-acetyltransferase (GCAT) 과 threonine dehydrogenase (TDH)는 미토콘드리아에서 glycine과 threonine 을 합성하는데 필요한 효소들이다. 이 과정 중 발생한 중간물질인 2-amino-3-ketobutyrate는 자연적으로 decarboxylation 되어 toxic metabolite인 aminoacetone로 바뀌는데, 원래 이 toxic metabolite는 TDH의 의해 제거된다. 하지만 인간에서는 TDH 유전자가 pseudogene 이고 실제 threonine dehydrogenase 활성도 없었다. 따라서 이 결과는 다른 후생생물과는 다르게 인간에서는 glycine이 threonine이 아닌 toxic metabolite인 aminoacetone으로 변환된다는 것을 의미한다 (그림 3). 본 연구실에서는 GCA가 TGLDC억제를 통해 증가된 glycine을 toxic metabolite인 aminoacetone을 변환한다는 것을 증명하고 이 pathway의 생리학적/ 병리학적 역할을 규명하는 연구를 수행하고 있다 (unpublished data).
|
|
4. Toxic metabolites in aging and neurodegeneration
본 연구실은 위에 제시된 암세포 특이적 metabolic pathway 뿐만 아니라 다른 다양한 질병 특히 neurodegenerative disorders와 aging 과 관련된 intermediate metabolite와 metabolic pathway 변이에 대한 연구도 수행하고 있다. 이러한 질병 관련 toxic metabolite pathways 규명함으로서 세포 대사과정을 이해하고 관련 질병 치료제 개발에 도움이 되는 연구를 하려고 한다.
Principal Investigator
|
Dohoon Kim, Ph.D. Assistant Professor, Department of Molecular, Cell and Cancer Biology Co-Director, Graduate Program in Cancer Biology Investigator, Suh Kyungbae Foundation
University of Massachusetts Medical School 364 Plantation Street, LRB room 422 Worcester, MA 01605 : 508-856-4428 : 508-856-1310 |
Lab Personnel

Lee – Postdoc
Anne Carlisle – Graduate student
Mihir Doshi – Graduate student
Austin Peppers – Graduate student
Meghan Spears – Graduate student
Selected publications
Lee N, Kim D. Cancer Metabolism: more than just growth. Cells. 2016 Dec 31; 3912): 847–854. Review.
Kim D, Fiske BP, Birsoy K, Freinkman E, Kami K, Possemato R, Chudnovsky Y, Pacold ME, Chen WW, Shelton LM, Gui DY, Kwon M, Kang SW, Snuderl M, Vander Heiden MG, Sabatini DM. SHMT2 survival in
Chudnovsky Y, Kim D, Zheng S, Whyte WA, Bansal M, Bray MA, Gopal S, Theisen MA, Bilodeau S, Thiru P, Muffat J, Yilmaz OH, Mitalipova M, Woolard K, Lee J, Nishimura R, Sakata N, Fine HA, Carpenter AE, Silver SJ, Verhaak RG, Califano A, Young RA, Ligon KL, Mellinghoff IK, Root DE, Sabatini DM, Hahn WC, Chheda MG. ZFHX4 interacts with the NuRD core member CHD4 and regulates the -initiating cell state. Cell Reports. 2014 Jan 30;62)313-24.
Possemato R, Marks KM, Shaul YD, Pacold ME, Kim D, Birsoy K, Sethumadhavan S, Woo HK, Jang HG, Jha AK, Chen WW, Barrett FG, Stransky N, Tsun ZY, Cowley GS, Barretina J, Kalaany NY, Hsu PP, Ottina K, Chan AM, Yuan B, Garraway LA, Root DE, Mino-Kenudson M, Brachtel EF, Driggers EM, and Sabatini DM. Functional genomics serine synthesis is essential in PHGDH-amplified breast cancer, Nature, 2011 Aug 18;4767360)346-50.
Sheen JH, Zoncu R, Kim D, Sabatini DM. Defective Regulation of Autophagy upon Leucine Deprivation Reveals a Targetable Liability of Human Melanoma Cells In Vitro and In Vivo. Cancer Cell. 2011 May 17;195)613-628.
Graff J, Kim D, Dobbin MM, Tsai LH. Epigenetic regulation of gene expression in physiological and pathological brain processes. Physiol. Rev. 2011 Apr912603-49. Review.
Kim D, Tsai LH. Bridging Physiology and Pathology in AD. Cell. 2009 June 12;1376)997-1000. Review.
Kim D, Frank CL, Dobbin MM, Tu W, Peng PL, Guan JS, Lee BH, Moy LY, Giusti P, Broodie N, Mazitschek R, Delalle I, Haggarty SJ, Neve RL, Lu YM, Tsai LH. Deregulation of HDAC1 by p25/cdk5 in Neuron. 2008 Dec 10;605)803-817.
Kim D*, Nguyen MD*, Dobbin MM, Fischer A, Sananbenesi F, Rodgers JT, Delalle I, Baur JA, Sui G, Armour SM, Puigserver P, Sinclair DA, Tsai LH. SIRT1 deacetylase protects against neurodegeneration in models for Alzheimer's disease and amyotrophic lateral sclerosis. EMBO J. 2007 Jul 11;2613)3169-79. *equal contribution)
Cruz JC*, Kim D*, Moy LY, Dobbin MM, Sun X, Bronson RT, Tsai LH. p25/cyclin-dependent kinase 5 induces production and intraneuronal accumulation of amyloid beta in J Neurosci. 2006 Oct 11;2641)10536-41. *equal contribution)