
생화학분자생물학회입니다.
키메라 항원 수용체(Chimeric Antigen Receptor, CAR)기반 항암면역 T세포치료제
작성자
관리자작성일자
2019-04-01조회수
2590키메라 항원 수용체(Chimeric Antigen Receptor, CAR)기반
항암면역 T세포치료제

김찬혁
KAIST 생명과학과 & 큐로셀 CTO
Kimchanhyuk@kaist.ac.kr
1. 서론
사람이 가지고 있는 고유의 면역 시스템을 이용한 질병 치료의 개념은 1700년대로 거슬러 올라간다. 영국의 의사였던 에드워드 제너(Edward Jenner)는 자신의
고향에서 근무하던 중, 소의 천연두인 우두에 감염되었던 사람들이 가볍게 앓고 나으면 천연두에 걸리지
않는다는 이야기를 듣게 되었고, 9세 때 우두를 앓았던 62세
존 필립의 자청을 통한 임상 실험을 통해 1798년 종두법을 발표하게 된다. 이후 1800년대 말 미국인 의사 윌리엄 콜리가 열을 가해 죽인
박테리아를 주입한 일부 환자에게서 암이 줄어드는 것을 관찰한 이후 환자의 면역계를 활용한 암 치료인 ‘항암면역치료’에 대한 연구가 계속돼 왔다. 2018년 노벨 생리의학상의 수상은 음성적 면역조절(negative
immune regulation) 억제에 의한 암 치료법을 개발한 James P. Allison과
Tasuku Honjo 교수에게 돌아갔다. 이들은 T 세포에 존재하는CTLA-4나 PD-1과
같은 수용체가 T 세포의 활성화를 억제하는 기능을 가지고 있음을 발견하였다. 그리고 이들 수용체의 기능을 항체를 이용하여 차단하였을 때 T 세포의
활성화가 회복되어 암세포를 정상적으로 공격하는 것을 확인하고, 이를 항암치료에 적용하였다. 이러한 면역관문요법(Immune checkpoint therapy)으로
불리는 치료법은 암에 대한 접근 패러다임 자체를 변화시키기에 이르렀다. 현재 이러한 임상적 성공의 선두에
위치한 항암 면역 치료제는 크게 세 부류로 1) 면역관문 수용체 차단항체, 2) 항 CD3항체 기반 이중 항체, 그리고 3) 키메라 항원 수용체(chimeric antigen receptor, CAR)를 발현하는 T 세포
치료제로 나뉠 수 있다. 이들 중 CAR-T 세포
치료제에 대한 관심이 최근 급증하고 있는데, B 세포 특이 항원인
CD19을 표적하는 CAR-T 세포 치료제 2종인
Tisagenlecleucel (Kymriah)와 axicabtagene
ciloleucel (Yescarta)의 경우 각각 B-cell ALL과 DLBCL 치료제로 2017년에 미국 FDA 승인을 받았고, 2018년 12월
기준 400건 이상의 임상 시험이 전 세계적으로 진행 중이다. 본
글에서는, 인간에 의해 디자인되어 만들어진 수용체인 CAR의
구조를 중심으로 CAR-T 치료제의 기본적인 원리와 효능, 안전성, 및 환자의 접근성을 향상시키기 위한 노력과, 나아가 항암제를 넘어
면역 조절을 통한 다른 인간 질병 치료에의 적응 가능성에 대해서 논의하려 한다.
2. 키메라 항원 수용체의 디자인
T 세포 수용체(T cell
receptor, TCR)는 α,β사슬로 이루어진 헤테로 다이머가 항원인식에 중요한 역할을 하고, 이는
T 세포 활성화에 중요한 ITAM (Immunoreceptor
tyrosine-based activation motif ) 도메인을 포함한CD3 ε, δ, γ, 그리고 ζ 사슬과 복합체를 이루고 있다 (그림 1좌). CAR의
경우엔 T 세포 활성화 CD3 ζ 도메인이 막관통 도메인을
통해 항체의 항원 선택적 scFv (single-chain variable fragment) 도메인과
하나의 폴리펩타이드로 연결되어 있고, 이러한 구조는 1세대
CAR로 명명되었다. 그러나 CD3 ζ신호만으로는 T 세포의 체내 증식과 지속성에 제한이 있다는 것이 관찰되어 추가적으로 보조 자극 수용체인 CD28 또는 4-1BB의 신호전달 도메인을 도입한 2세대 CAR, 그리고 여러 종류의 보조 자극 수용체 도메인을 동시에
도입한 3세대 CAR의 구조로 진화하였다. (그림 1)
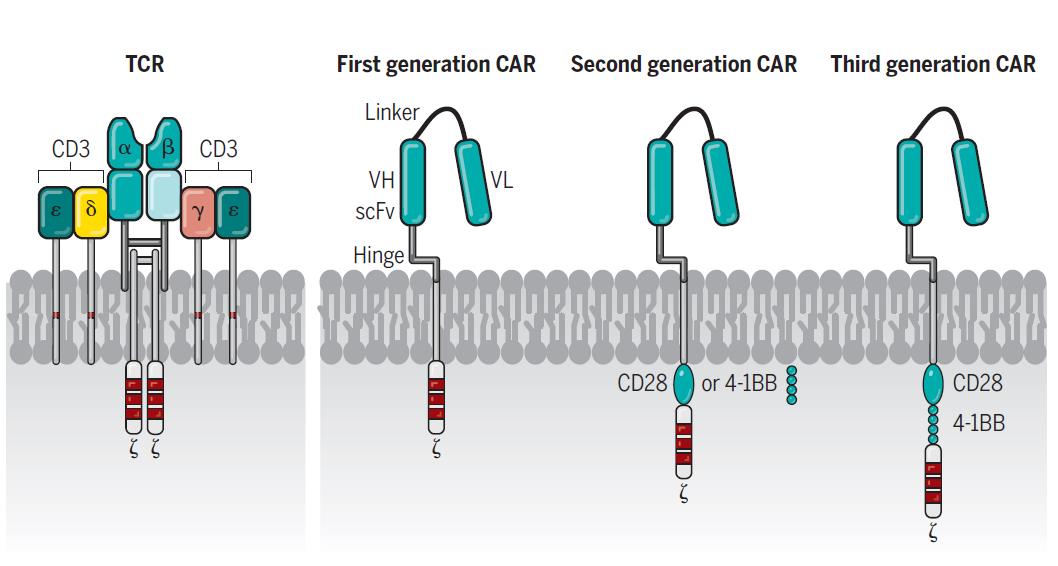
그림 1. T 세포의 항원 수용체 (왼쪽)와 CAR 수용체 (오른쪽) [Science 2018, 359: 1361-1365]
이러한 CAR는 기본적으로 1) 표적 도메인, 2) 연결 도메인, 3) 막관통 도메인, 그리고 4) 신호전달 도메인으로 구성되어 있고 각각의 요소들은 CAR의 효율적인 발현뿐만 아니라 CAR-T 세포의 항암 효능과 안전성에 큰 영향을 미칠 수 있다.
2.1. 표적 도메인 (Targeting Domain)
TCR의 경우 일반적으로 HLA(Human
Leukocyte antigen) – peptide complex를 통해 표적 세포를 인지하는 반면,
CAR는 항체에서 유래한 항체 단편(scFv)을 주로 이용하기 때문에 암세포 표면에 과발현되는
단백질뿐만 아니라 당사슬(e.g. Lewis Y)과 당지질(e.g. GD2)에
이르기까지 다양한 종류의 항원을 인식할 수 있다.
CAR에 대한 최적의 항원결정기(epitope)를
찾을 수 있는 규칙은 현재 일반화하기가 매우 어렵다. TCR의 경우 HLA-peptide
complex인지 시에는 T 세포와 표적 세포 간의 거리가 대략 13~15 nm로 일정하게 유지된다. 이러한 거리는 T 세포가 표적 세포를 인식하여 소위 면역 시냅스(immunological
synapse)를 형성하였을 때, T 세포에서 최적의 활성화를 유도하는데 매우 중요한 역할을
하는 것으로 보고되고 있다. CAR의 경우 매우 다양한 표적 도메인과 항원 결정기 간의 인식에 의해
신호전달이 이루어져야 하므로, CAR-T 세포와 표적 세포와의 거리는 큰 영향을 받게 된다. 따라서, 항원 내에서 scFv가
인식하는 항원결정기의 상대적인 위치와, scFv와 막통과 도메인을 연결하여 주는 이른바 연결 도메인의
길이와 형태가 CAR -T의 최적의 활성화를 유도하는데 매우 중요한 작용을 할 것이라 사람들이 판단하고
있다. 이를 뒷받침하는 결과 중 하나로 동일한 CD22 항원을
표적하는 항체들 중에 에피토프의 위치가 상대적으로 세포막에서 가까운 쪽을 인식하는 scFv를 사용하였을
때 CAR-T 세포의 활성화가 더욱 효율적으로 일어나는 것이 보고되었다. 하지만 아직까지 CAR의 항원 결정기와의 결합 친화도, 항원의 발현 정도, 항원의 특정 위치에서의 밀도 등의 CAR-T 세포의 선택성에 미치는 영향에 대한 연구가 미미한 실정이다.
생쥐의 서열에 기반한 scFv를 사용한 CAR-T 세포치료제의
경우에는, 반복 투여시 환자의 몸 안에서 심각한 과민증(anaphylaxis)을
일으켜 안전성에 영향을 미칠 수 있다는 것이 보고된 바 있다. 뿐만 아니라 면역 원성이 CAR-T 세포가 체내에서 지속되는 기간을 감소시킬 수 있음을 시사하는 임상시험 결과 또한 보고되었다. 이러한 면역원성의 문제를 극복하기 위해서는 항체 서열의 인간화 과정을 거치거나, 인간서열 항체를 발현하는 유전자조작 생쥐 혹은 디스플레이 라이브러리로부터 새로이 항체를 발굴하는 시도가 가능하다.
암세포에 과발현하는 암관련항원(tumor-associated antigens, TAA)은 많은
경우 일반세포에서도 낮은 수준으로 발현하고 있다. 따라서 CAR-T 치료제의 on-target off-tumor 부작용은 환자에게서 심각한 결과를 초래할 수 있다. 일례로 여러 암에서 일부 과발현되는 것으로 잘 알려진 HER2 단백질을
표적하는 CAR-T 세포를 전이성 대장암 환자에게 주입하였을 때, 폐
안에서 낮은 수준으로 발현하는 HER2를 인식하여 활성화됨으로써 환자를 사망에 이르게 한 경우가 보고되었다. CAR-T의 증가된 항원 민감성에 의해 발생하는 부작용을 줄이기 위한 노력으로, 항체의 항원 인식부위에 돌연변이를 도입하여 원조 단일 클론 항체에 비해 고의적으로 친화력을 낮춘 시도들이 보고되었다.
2.2. 연결 도메인 (Spacer Domain)
연결 도메인은 표적 도메인으로 하여금 CAR-T 세포막 과의 일정 거리를 두고 보다 유연하게 표적 항원을 인식할 수 있도록 도입되었다. 지나치게 길이가 긴 연결도메인은 CAR-T의 활성화에 부정적인 영향을 미칠 수 있지만, 다른 한편으로는 항원의 크기가 큰 경우 표적 도메인의 원활한 접근을 위해 일정 길이 이상의 연결 도메인이 필요할 수 있다.
최근 CAR 디자인에 주로 사용되는 연결도메인 서열들은
CD8a나 CD28의 hinge 부위, 혹은 항체(IgG1 혹은
IgG4)의 Fc 부위 등이 있다. CD28과 CD8 hinge를 차용한 연결 도메인은 대략 40여 개의 아미노산으로
이루어지며 특정한 3차 구조를 이루지 않는데 비해, 항체의 Fc(CH2와 CH3)를 이용한 연결 도메인은 200개 이상의 아미노산을 포함하며 immunoglobulin fold로
이루어진 3차 구조를 갖는다. 이러한 잘 접혀진3차 구조로 인해 현저히 많은 아미노산 숫자에도 불구하고 Fc 기반
연결 도메인은 CD8a 나 CD28 hinge에 기반한 연결
도메인에 비교했을 때 유사한 길이를 갖게 될 것으로 추측할 수 있다. 이외에도 CD8 혹은 CD28 hinge는 서열 안에 존재하는 시스테인 잔기에
의존하여 CAR homodimer를 이루는 반면, Fc 기반
연결 도메인은 추가적인 단백질-단백질 상호작용(protein-protein
interaction)을 통해 더욱 강하게 CAR homodimer를 이룰 수 있다.
2.3. 막관통 도메인 (Transmembrane Domain)
막관통 도메인은 세포막 외부의 연결 도메인과 세포막 내부의 신호전달 도메인을 연결하는 역할을 하며 CAR 발현양에 큰 영향을 미칠 수 있다. 최근 보고되는 CAR의 디자인에 사용되는 막관통 도메인은 CD8a와 CD28의 서열에서 차용된 것들이 주를 이루고 있다. 초기 1세대 CAR의 디자인에는 CD3 zeta 도메인의 막관통 도메인이 사용되었는데, 이러한 CAR는 T 세포에 존재하는 CD3-zeta 사슬과 heterodimer를 형성하며 내재적인 TCR과 상호작용할 수 있음이 보고되었다.
TCR을 비롯한 여러 활성 면역 수용체들(e.g. NKG2D, FcRs, TREM2 etc.)은
많은 경우 세포 밖의 리간드를 인식하는 부위와 세포 내의 신호전달을 담당하는 부위가 비공유적으로(non-covalently)
연결된 복합체를 형성하고 있다. 이때, 막관통
도메인들은 이온 결합 등을 통해 두 부위가 상호작용을 하는데 중요한 역할을 한다. 이러한 성질을 이용하여
서로 다른 막관통 도메인을 조합함으로써 단일 폴리펩타이드가 아닌 두 개 이상의 폴리펩타이드의 복합체로 이루어진 형태의 CAR를 디자인하는 것이 가능하다.
2.4. 신호전달 도메인 (Signaling Domain)
1세대 CAR 디자인에서는 신호전달 도메인으로서 CD3-zeta 혹은 Fc receptor γ와 CD8, CD4, CD25 혹은 CD16을 연결하여 phosphatidylinositol, tyrosine kinase pathway를 거쳐 calcium influx 를 유도하도록 CAR가 고안되었다. 이들 CAR-T 들은 체내에서 증식과 장기간 생존이 제한되어, 임상에서 인상적인 효능을 보여주지 못하였다. 이를 극복하기 위하여 CD28 또는 41BB(CD137)와 같은 보조 자극 수용체의 신호전달 부위를 CD3-zeta에 추가한 것이 “2세대” CAR-T로 불린다. 실제로 CD28이나 41BB에 기반한 2세대 CAR-T들은 생체 내에서 급격하고 왕성한 증식과 오랜 생존 능력을 보였는데, 이러한 특징은 매우 향상된 항암효과로 연결되었다. 그 결과 현재까지 미국 식약청의 허가를 받은 두 종의 CAR-T인 노바티스사의 Kymriah와 길리어드사의 YESCARTA는 각각 41BB 혹은 CD28 신호전달 도메인에 기반한 것이다.
CD28과 41BB는 세포막 수용체들로, 리간드
결합 시 둘 모두 CD3의 신호를 보강하며 세포사멸 관련 인자들을 억제한다는 공통점을 가지고 있다. 그러나 두 단백질은 구조적으로 매우 다른 그룹(CD28 family vs
TNFR family)에 속할 뿐만 아니라, 이들 수용체들과 밀접하게 상호작용하며 활성의
조절과 신호전달에 관여하는 단백질들의 부류 또한 매우 다르다. 2세대
CAR-T 치료제에서 한걸음 더 나아가, 서로 다른 두 종류의 보조 자극 수용체를 조합한
‘3세대’ CAR-T 들이 개발되었다. 그러나 3세대가 실제로 2세대에
비해 향상된 항암 효능을 갖는가에 대해서는 서로 엇갈린 결과들이 보고되고 있다. 또한 일부 실험 결과들에
따르면 두 종류의 costimulatory 신호 전달 부위가 하나의 폴리펩타이드 사슬로 연결되었을 때
각각이 완벽하게 작동하지 않을 가능성을 배제할 수 없다. 이를 극복하기 위해서는 두 종류의 costimulatory 신호를 서로 다른 폴리펩타이트 사슬로 분리해 배치하는 디자인이 가능하다.
T 세포의 최적의 활성화를 위해서는 3종류의 신호(TCR, costimulatory, 그리고 사이토카인)를 함께 전달하는 것이 이상적이다. 이를 위해 2A 혹은 IRES와 같은 시스템을 이용해 원하는 사이토카인 유전자를
CAR와 동시에 발현하는 시도들이 보고되었다. 그러나 이러한
디자인으로 만들어진 CAR-T 세포는 사이토카인을 항상 발현하는 상태이므로 체내에서 독성을 유발할 위험이
있다. 이를 극복하기 위해서 CAR의 디자인 내부에 IL2 수용체 beta chain의 일부를 삽입하고 CD3-zeta에 돌연변이를 도입함으로써, CAR-T 세포의 내부로만
항원 의존적으로 STAT3와 STAT5 신호를 전달하는 디자인이
개발되었다.
3. 임상에서의 CARs
3.1 CD19-표적 CAR-T cell
1세대 CAR-T의
경우 임상에서의 결과가 그리 좋지 않았으나, 2011년 CD19를
표적으로 하는 2세대 CAR-T의 경우 놀라운 결과를 보여
T세포 치료제 개발에 패러다임 변화를 가지고 오게 되었다. CD19의
경우 거의 모든 B 세포의 발달 단계에서 발현하는 반면, 다른
세포에는 발현양이 매우 제한적이므로 표적 치료의 관점에서 이상적인 항원으로 여겨진다. 또한 CD19-표적 CAR-T 치료에 따른 정상 B 세포의 결핍으로 인한 부작용은 항체(IVIG)의 정맥주사를 통해 보완이 가능하다는 장점이 있다. 하지만
매우 우수한 임상 효능에도 불구하고, CAR-T 세포의 주입 후 체내에서 급격하게 일어나는 T 세포의 증식에 동반하는 cytokine release syndrome
(CRS), 아직 구체적인 원인을 알 수 없는 신경독성, 그리고 장기간에 걸친 B 세포 결핍 등 아직 해결해야 할 CD19-표적 CAR-T 치료제의 부작용이 존재한다.
3.2 CAR-T for solid tumors
CD19이 아닌 다른 표적에 대해 성공적인 CAR-T들이 보고 되고 있으나 대부분의 경우 혈액암 계통에 대한 치료제들이다. (BCMA for multiple myeloma, CD22 for B cell malignancie 등 현재까지 잘 알려져 있는 고형암에 대한 여러 항원들 (ERBB2/HER2, carbonic anhydrase IX, EGFRvIII, mesothelin, carcinoembryonic angtigen, GD2 ganglioside 등)을 표적으로 하는 CAR-T들이 시도되었으나, 혈액암 치료 효과에 버금가는 결과는 아직 보고되지 않고 있다. 고형암에서 CAR-T 치료제가 제한적인 효과를 보이는 이유로는 면역억제적인 종양미세환경(tumor microenvironment)과 암세포의 이질성(heterogeneity) 뿐만 아니라, 혈액암에 비해 상대적으로 CAR-T 세포의 침투가 어려운 점 등을 들 수 있다. 따라서 이를 극복하기 위한 여러 전략들이 시도되고 있는데, 예를 들어 면역관문 신호에 의해 CAR-T 세포가 불활성화되는 것을 극복하기 위해 PD-1/PD-L1 억제 항체를 병용 투여하는 전략이 시도되고 있다.
3.3. 자가유래 CAR-T 치료제 개발의 어려움
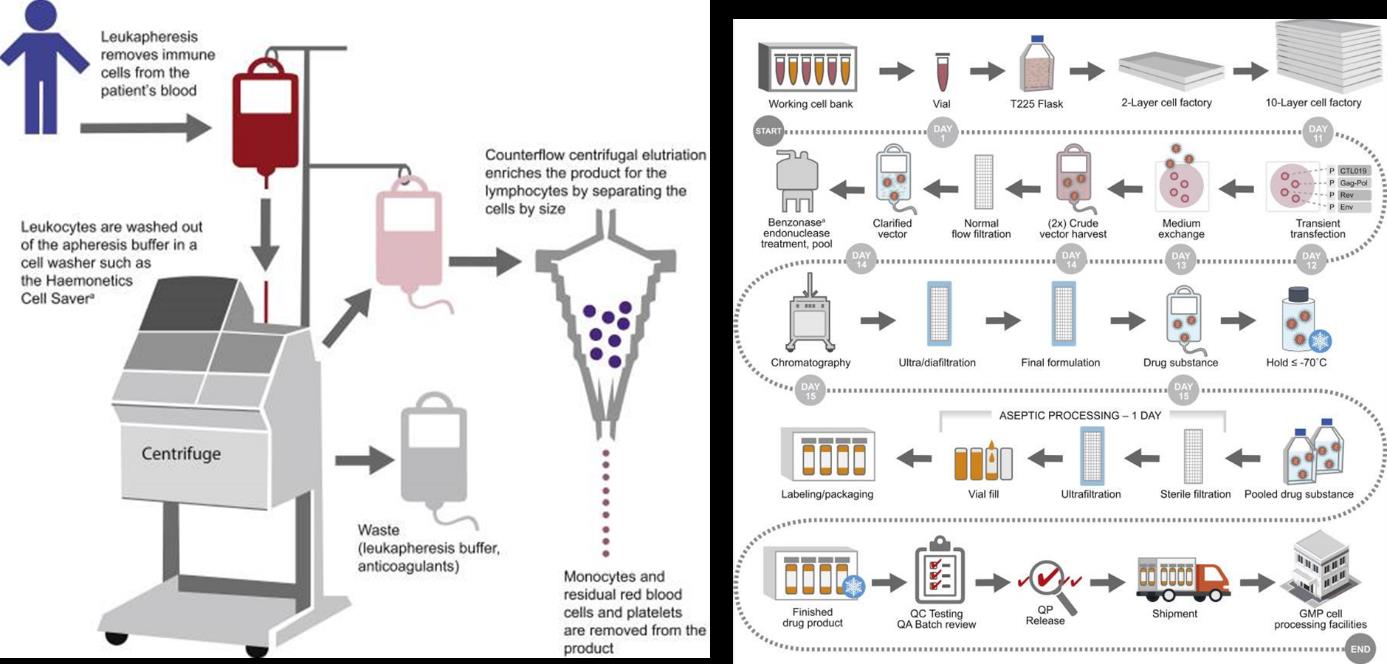
그림 2. 백혈구성분채집술 (Leukapheresis) (좌) 및 Lentiviral vector를 활용한 (우) CAR-T 제조과정 [Mol Ther Methods Clin Dev 2017, 4: 92-101]
현재 허가받은 CAR-T 치료제는 모두 자가유래 맞춤 치료제로 생산공정이 복잡하여 품질관리가 어렵고, 적시에 환자에게 치료제를 공급하는 것이 쉽지 않다. (그림 2). 또한 자가유래 CAR-T는 복잡한 제조 특성으로 인해 다른 치료제 대비 가격이 상당히 높아, 현재 승인된 CD19-표적 CAR-T 치료제의 경우 1회 투여 비용이 $350,000- $500,000이며, 여기에 부작용 및 사후 관리 비용까지 계산하면 천문학 적인 비용이 소모된다. 이들 CAR-T 치료제는 원료에 해당하는 T 세포를 모두 환자 말초 혈액에서 분리해서 사용하고 있기 때문에 제작된 CAR-T 세포 간의 상당한 질적 및 양적 차이가 존재한다. 이를 극복하기 위해 동종유래 CAR-T를 사용하는 것이 가능하다. 예를 들어 유전자 편집술을 활용하여 TCR이 제거된 공여자 유래 CAR-T를 만들어 여러 환자에게 투여하는 것이다) 이러한 전략의 경우 이식편대숙주병(graft versus host diseases(GvHD))의 부작용이 일어남을 확인하였는데, 이는 유전자 편집 효율에 따른 것으로 판단되어 CRIPR 등 유전자 편집 효율이 좋은 기술을 활용한 시도들이 계속되고 있다.
4. 보다 나은 CAR-T 치료제를 만들기 위한 노력
효과적인 암세포 제거의 관점에서 이상적인 CAR-T 세포의 형질은 1) 면역 억제적 환경에서도 암세포에 대해 높은 살상 능력을 보이며, 2) 항원
특이적으로 뛰어난 증식능을 보이고, 3) 일정 기간 이상 체내에서 유지되는 생존 능력을 갖는 것이다. 이러한 CAR-T 치료제를 만들기 위해 CAR의 디자인 못지않게 중요한 것은 T 세포 자체이다. 예를 들어, 만성 백혈성 환자의 몸에서 분리된 T 세포가 이미 탈진된 형질을 보일 경우 이를 통해 만들어진 CAR-T 치료제의
효과가 저해될 수 있음이 최근 보고되었다. 이러한 탈진된 T 세포를
엔지니어링을 통해 어떻게 reinvigorate 시킬 수 있을 것인가는 앞으로 해결해야 할 중요한 과제이다. 또한 동일한 T 세포로 만들어진
CAR-T 세포일지라도 배양조건에 따라 더욱 “젊은” 형질(e.g. TCM)을 유지하며, 이것이 체내에서 더욱 왕성한 증식과 향상된 항암 효과로 이어진다는 것이 보고되었다.
현재까지 CAR-T의 표적도메인으로 사용되는 scFv들은
대부분 기존 단일클론 항체의 서열을 이용하여 제작되었다. 단일클론 항체들은 일반적으로 최초의 수많은
후보 서열들로부터 단백질 치료제로서의 용도를 고려하여 다양한 기준들(친화력, 항원 선택성, 이종 항원인식, 생물리적
특성, 반감기 등)을 통과하고, 이후 단일클론 항체 형태로 효능 시험을 거친 후에 선택된다. 그러나
이러한 항체의 선별 기준들 중 일부는 CAR-T 세포 치료제에 적용되었을 경우 무관하거나 상반된 영향을
미칠 수 있는 반면, CAR-T의 효능에 결정적 영향을 미치는 것으로 알려진 요인들(e.g. 에피토프의 위치)이 고려되지 않는 경우가 많다. 따라서 향후 CAR-T의 효능에 최적화된 scFv를 발굴하기 위해서는 새로운 전략의 수립이 필요하다.
이에 대한 대안으로 Piggy-back이나
Sleeping Beauty와 같은 transposon 시스템을 이용하여 DNA플라스미드 형태로 CAR 유전자를 전달하는 방법이 개발되어 임상에서
시험되고 있다. 더 나아가, transposon 시스템이 CAR 유전자를 무작위적으로 삽입하는 문제를 해결하기 위해, CRISPR 등과
같은 유전자 편집 도구를 이용해 CAR 유전자를 genome 상의
특정 위치에 삽입하는 시도들이 보고되었다. 특히 이러한 유전자 편집 도구를 이용한 위치 특이적(site-specific) 삽입 방법은 원하는 CAR 유전자의 삽입과
동시에 원하지 않는 유전자를 제거할 수 있다는 점에서, CAR-T의 효능 향상 또는 동종 타가유래 CAR-T의 제작과 같은 목적을 동시에 달성할 수 있는 잠재력을 갖고 있다. 그러나
이러한 유전자 편집을 위해서는 먼저 DNA의 이중나선에 결손이 일어나야 하는데, 이로 인해 대표적인 종양 억제 단백질인 p53의 활성화가 일어나
삽입 효율이 감소하는 것이 보고되었고, DNA의 large
deletion 혹은 translocation 이 일어나는 등, 아직 안전성에 대한 우려가 존재하고 있다.
최근 들어 T 세포뿐만 아니라 CAR 유전자를
NK, gamma delta T, NKT와 같이 세포 독성능을 가진 면역세포들 혹은 대식세포에 도입하여
항암면역 세포치료제로 활용하려는 연구 및 개발이 활발히 이루어지고 있다. 또한 CAR-T 세포를 이용하여 병원성 면역세포를 제거하거나, 혹은 CAR를 조절 T 세포(Treg)에
도입하여 자가면역 질환 및 장기이식에 적용하는 것이 가능하다. 이와 같이 면역세포의 엔지니어링 개념은
비단 암뿐만 아니라 자가면역, 과민반응, 장기이식, 더 나아가 대사질환 및 퇴행성 신경 질환과 같이 면역계와 밀접하게 관련된 질환의 치료제 개발에 폭넓게 적용될
수 있는 잠재력을 가지고 있다.
4. 맺음말
T 세포의 내재적인 수용체인 TCR을 본떠 디자인한 인공 수용체인 CAR는, 자연계에 존재하는 면역기능을 능동적으로 변형시켜 새로운 종류의 치료제 개발에 적용한 합성 면역학적 연구 결과의 결정체라 할 수 있다. 이제껏 본 글에서 언급된 CAR 디자인의 고려 사항 중 일부는 T 세포를 이용한 항암치료제의 경우에 국한된 것일 수도 있다. 예를 들어, NK 세포에서 최적의 효과를 보이는 신호전달 도메인의 조합은 T 세포의 그것과 다를 수 있다. 뿐만 아니라, 체내에서 폭발적으로 증가하는 CAR-T 세포의 형질은 말기 암 환자의 몸속에 존재하는 엄청난 숫자의 암세포에 대적하기 위해서는 필수 불가결한 요소이지만, 다른 질병의 경우 그 중요성이 상대적으로 낮을 수 있다. 결론적으로, 향후 CAR 유전자는 적용하려는 세포와 치료하려는 질병의 목적에 맞게 최적화되어 “진화”할 것이다.
참고문헌
1. Oiseth, S. J., Aziz, M. S. (2017) Cancer immunotheraphy: a brief review of the history, possibilities, and challenges ahead. J Cancer Metastasis Treat 3:250-61.
2. Smith, A. J., Oretle, J., Warren,
D., Prato, D. (2016) Chimeric antigen receptor (CAR) T cell theraphy for
malignant cancer: Summary and perspective. Journal
of Cellular Immunotheraphy 2: 59e68.
3. Pettitt, D., Arshad, Z., Smith,
J., Stanic, T., Holländer, G., Brindley, D. (2018) CAR-T Cells: A Systematic
Review and Mixed Methods Analysis of the Clinical Trial Landscape. Mol Ther 726:342-353
4. Zhang, E., Xu, H. (2017) A new
insight in chimeric antigen receptor-engineered T cells for cancer
immunotherapy. Journal of Hematology
& Oncology 10:1-11
5. Cerwenka, A. and Lanier, L. L.
(2016) Natural killer cell memory in infection, inflammation and cancer. Nature Reviews Immunology 16: 112–123
6. Kathy S. Wang, K. S., Frank,
D. A., and Ritz, J. (2000) Interleukin-2 enhances the response of natural
killer cells to interleukin-12 through up-regulation of the interleukin-12
receptor and STAT4. Blood 15, 95(10):3183-90
7. Muntasell, A. and Lopez-Botet,
M. (2016) Natural Killer Cell Based Immunotherapy in Acute Myeloid Leukemia:
Lessons for the Future. Clin Cancer Res
22(8): 15.
8. June, C. H., O’Connor, R. S., Kawalekar,
O. U., Ghassemi, S., Milone, M. C. (2018) CAR T cell immunotherapy for human
cancer. Science 359: 1361-1365.
9. Brentjens, R. J. et al., (2013)
CD19-targeted T cells rapidly induce molecular remissions in adults with
chemotherapy-refractory acute lymphoblastic leukemia. Sci Transl Med 5: 177ra38.
10. Levine, B. L., Miskin, J., Wonnacott,
K., Keir, C. (2017) Global Manufacturing of CAR T Cell Therapy. Mol Ther Methods Clin Dev 4: 92-101
첨부파일