
생화학분자생물학회입니다.
초희귀질환의 유전체 연구를 통한 정밀, 맞춤의학
작성자
관리자작성일자
2016-04-01조회수
1352초희귀질환의 유전체 연구를 통한 정밀, 맞춤의학
![1458881176_[4월호] Translational Research -저자사진.jpg](../../data/ksbmb_data/images/smarteditor/1458881176_[4월호] Translational Research -저자사진.jpg)
최무림
서울대학교 의과학과
murimchoi@snu.ac.kr
1. 희귀질환이란?
매년 2월 마지막날을 ‘희귀질환의 날 (Rare Disease Day)’이라고 한다. 올 2월 29일에도 희귀질환 관련 기관, 회사들은 각종 홍보 자료를 배포하였고 최근 유행에 맞게 멋진 인포그래픽스로 희귀질환에 대한 대중의 관심을 촉구하였다. 특기할만한 점은, 각 자료에서 이구동성으로 내세운 문구가 ‘희귀질환은 희귀하지 않다 (Rare Diseases are not rare)’는 것이다. 비록 질환 하나하나의 유병률은 낮지만 현재까지 약 6,000개가 넘는 질환의 종류가 알려져 있고 이렇게 다양한 질환들을 모두 아우르다 보면 상당히 많은 사람들이 적어도 하나의 희귀질환의 영향에 놓이게 될 것이다.
여러 질환을 빈도로 분류할 때, 약 2천명 중 한 명꼴로 발생하는 질환을 희귀질환 (Rare Disease)이라고 하며, 약 5만명 중 한 명꼴로 발생하는 질환을 초희귀질환(Ultra-Rare Disease)라고 한다. 하지만 이러한 분류의 기준은 나라마다 다르기에 절대적인 수치는 아니다. 희귀질환의 각종 통계는 다음과 같다.
미국의 경우 약 3천만명의 사람들이, 영국의 경우 약 3 50만명 정도의 사람들이 희귀질환에 의하여 고통받고 있다고 한다.
- 6%의 사람들은 일생동안 한 번 정도 희귀질환의 영향 아래에 있게 된다.
- 30%의 희귀질환 환자는 5살이 되기 전에 사망한다.
- 50%의 희귀질환 환자는 소아이다.
- 80%의 희귀질환은 유전적인 원인에 의한 것이다.
- 80%의 희귀질환 환자들은 연구에 적극적 참여 의사가 있다.
- 95%의 희귀질환은 FDA에서 허가된 약이 없는 상태이다.
- 평균적으로 희귀질환 환자들은 약 3번의 오진을 받으며, 약 4년이 지나야 진단을 받게 된다. (“Diagnostic Odyssey” 라고도 함)
- 미국의 경우, 한 명의 희귀질환 환자에 의하여 평생 발생되는 의료비는 약 5백만달러로 추산된다.

그림 1. 올해 2월 29일 Rare Disease Day를 기념하여 나온 인포그래픽스 포스터 (http://www.rarediseaseday.org)
즉, 희귀질환은 유전적인 영향이 크며 그렇기 때문에 대부분은 소아 환자들이고, 각 질환에 의하여 고통받는 환자의 수는 적지만 많은 종류의 질환이 있기 때문에 이를 모두 합하여 다양한 원인에 의하여 고통을 받고 있는 상태이다. 초희귀질환은 그 중에서도 그 희귀성으로 인하여 별다른 주목을 받지 못하던 상황이었으나 최근 유전학의 발전으로 보다 활발한 연구와 치료의 대상으로 주목받고 있다.
실제 미 보건원 산하 인간유전체연구소 (NHGRI: National Human Genome Research Institute)의 Eric Green소장은 유전체 연구가 점점 활기를 띠고 있던 2014년, 6가지의 ‘핫 토픽’ 을 언급하였으며 초희귀질환의 진단과 적극적 치료가 그 중 한가지 주제로 꼽히기도 하였다. 이에 발맞추어 NHGRI에서는 기존의 UDP 프로그램을 업그레이드 시킨 UDN 프로그램을 개시하였다.
2. Undiagnosed Disease Program (UDP) / Undiagnosed Disease Network (UDN)
UDP는 NHGRI에서 2008년 시작하여 2015년 종료된 프로그램으로 기존의 임상적 카테고리에 들어가지 않는, 진단되기 힘든 경우의 환자들을 대상으로 시스템적인 임상, 유전적 분석을 수행하여 환자가 걸린 병에 대한 진단을 내리고 그 증상의 원인을 찾아보려는 노력이다. NIH의 병원에서 환자의 임상적, 분자생물학적 평가를 거쳐 기존 질환에 맞는 진단을 하거나, 혹은 새로운 질환으로 분류를 하였다. 동시에 그 증상의 원인을 유전적인 분석으로 알아보기도 하였다. 연구 기간 동안 2,954건의 지원이 있었으며 그 중 853건이 실제 연구 대상으로 인정이 되었다 (~30%). 성공적인 UDP의 수행 이후 미 정부는 UDN이라는 후속 프로젝트를 시작하였다 (그림 2).
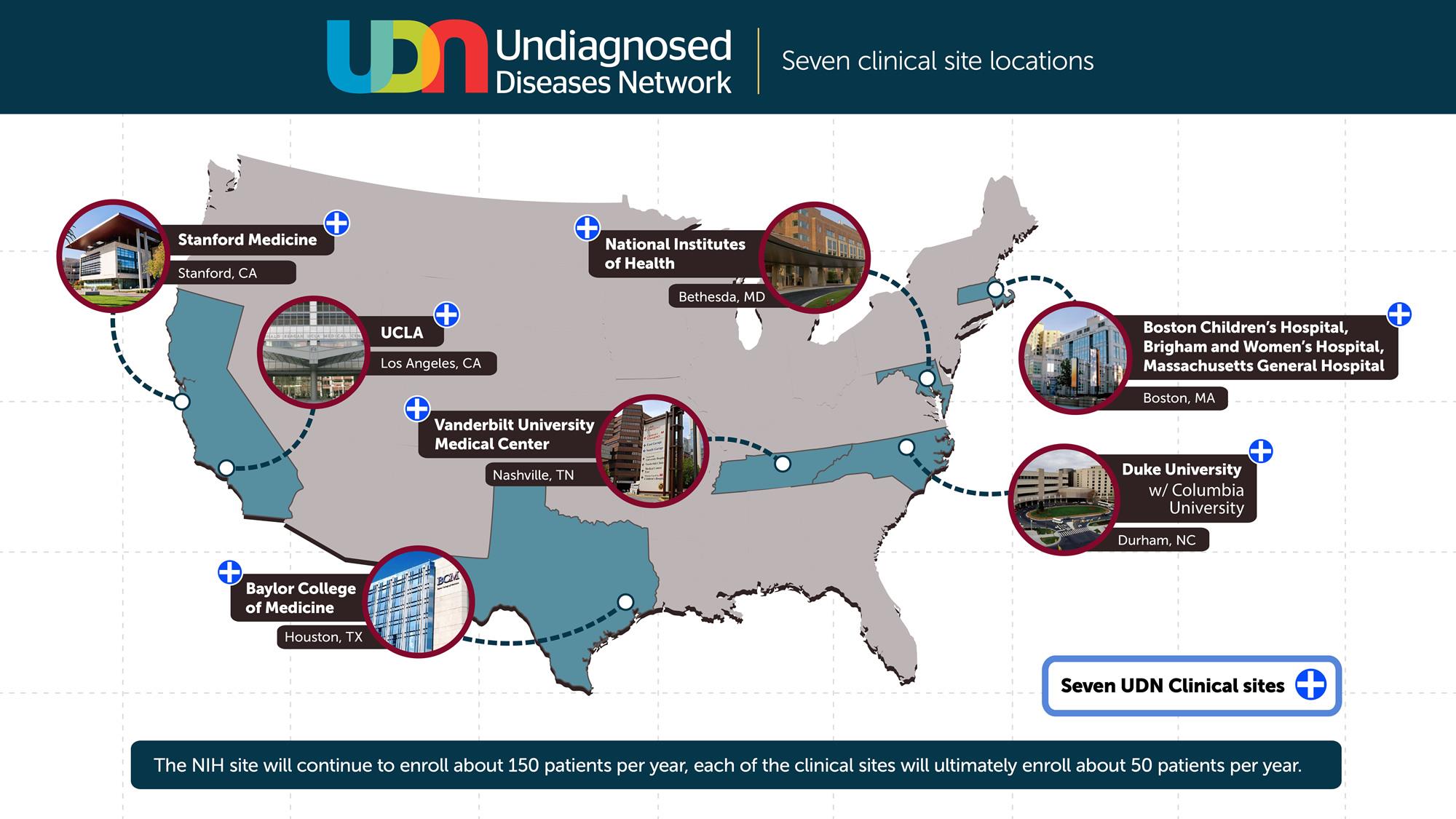
그림 2. UDN 프로젝트 참여 기관 목록 (http://www.genome.gov)
UDN에서는 현재 6군데의 임상 센터를 더하였고 DNA 시퀀싱 센터, 모델 동물 센터, 대사체 센터, 조직은행 등의 각종 센터들을 종합하고 있다. 최근 발표된 논문에 이러한 미 정부의 노력의 성과물이 자세히 보고되고 있다. 즉, (1) 복합질환 이해의 실마리 부여, (2) 새로운 질환 발생의 기작 이해, (3) 두개 이상의 희귀질환이 겹친 경우, (4) 정밀의학의 예시가 될만한 케이스들이 각각 항목별로 나열되었다. (그림 3, Gahl et al. 2016)
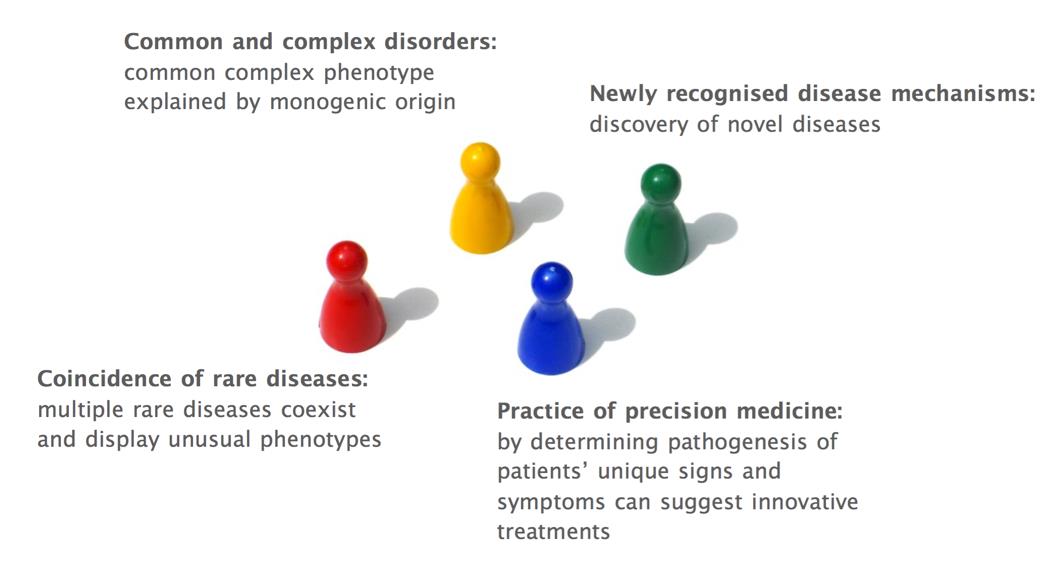
그림 3. UDP/UDN 프로젝트에 의하여 발생하는 지식적 성과의 종류 (Gahl et al.내용 바탕으로 작성)
3. 유전체 연구를 통한 초희귀질환의 이해
약간의 무리가 있지만, 이해의 목적을 위하여 1941년 Beadle과 Tatum이 Neurospora를 대상으로 한 실험 결과를 바탕으로 주장했던 ‘One-Gene One-Enzyme’ 개념을 현재의 분자유전학적 개념에 대입 해 보겠다. 아직 정확한 수를 알 수는 없겠지만, 유전체 상에는 Isoform을 제외하고 약 2만개 남짓한 유전자가 있다고 알려져 있다. One-Gene One-Enzyme의 개념을 적용한다면, 그 2 만여개의 유전자가 각각 돌연변이를 가지게 될 때 각 경우에 특별한 다양한 세포 수준의, 조직 수준의, 혹은 개인 수준의 문제를 일으킬 수 있을 것이라고 가정할 수 있을 것이다.
위에서 80%의 희귀질환은 유전적인 원인에 의하여 발병한다고 하였다. 즉 인간이 가지고 있는 유전자들 중 어떤 유전자의 단백질 합성 부분, 혹은 유전자 조절 부분에 생긴 돌연변이가 각종 문제를 일으켜 환자의 여러 증상을 유발시킨다고 하였을 때 그 돌연변이와 유전자의 기능, 그리고 그것에 문제가 생겼을 때에 생기는 결과의 정보가 최근 환자 기반의 유전체 연구를 통하여 속속들이 밝혀지고 있다.
(Chong et al., 2015). 위에서 설명한 UDP/UDN 프로젝트처럼 초희귀질환 환자들을 대상으로 하는 연구는 아니지만 역시 NIH/NHGRI에 의하여 미국에서 수행되고 있는 희귀질환 대상 Mendelian Center 프로젝트의 논문에 따르면 전체 유전자들 중 약 15% 정도가 돌연변이가 생겼을 때 각종 Mendelian Disease를 유발시키는 것으로 알려졌으며, 약 30% 정도의 유전자들은 돌연변이가 생겼을 때 더 심각한 문제를 일으켜 배아 발생 동안의 문제 때문에 아예 태어나지 못하게 하는 경우이다. 나머지의 유전자, 약 만 개 정도는 아직 그 역할이 확실히 밝혀지지 않았거나 돌연변이가 있어도 별다른 증상을 나타내지 않는 경우로 남아있는 상태이다. 하지만 최근 유전체학의 연구에 의하여 나머지 유전자들의 실제 사람에서의 역할이 속속들이 밝혀지고 있다. 한 가지 방법은, 건강한 사람들에게서 knockout 된 유전자들을 찾는 것이다. Human Knockout Project라도고 부르는 이러한 노력들에 의해서 여러 유전자들이 실제로 사람들에게서 knockout되더라도 별다른 임상적인 문제점을 일으키지 않는 것으로 알려지고 있다 (Alsalem et al., 2013; Sulem et al., 2015). 반대로, 기존에 보기 힘든 증상을 가진 환자들의 유전체를 연구하여 돌연변이를 찾아내고 그 변이의 역할을 연구하여 그 유전자의 새로운 역할을 알 수 있을 것이며, 운이 좋다면 그 돌연변이를 조절할 수 있는 약을 투여하여 환자의 증상 호전을 기대할 수도 있을 것이다. 아래에는 실제 그러한 연구 결과에 대해 설명하겠다.
4. CTLA4 돌연변이를 가진 자가면역증 환자
본 연구의 대상이 된 초희귀질환 환자는 현재 14세 여아이며 신생아 때부터 자가면역 증세에 의하여 극심한 장질환에 의한 설사와 빈혈, 간염 등의 증상으로 고통을 겪어왔으며 12세라는 어린 나이에 위암에 걸리기도 하였다 (Lee et al., 2016). 특히 자가면역성 장질환으로 인하여 장이 제 기능을 하지 못하여 하루에 3리터씩의 설사를 하고 있었다. 여러 자가면역 질환의 카테고리에 맞지 않아 확실한 진단을 받지 못하여 고생을 하고 있었고, 이에 환자와 건강한 부모의 유전체를 whole exome sequencing으로 분석, 환자가 특이적으로 가지고 있는 유전적 돌연변이를 찾았으며 이는 CTLA4 라는 유전자상의 염기 치환이었다.
CTLA4는 면역세포상에 위치하여 면역 활성화를 조절하는 역할을 하는 단백질이며 우리 환자의 돌연변이는 CTLA4로 하여금 면역 활성화 조절을 못하게 하는 역할을 하는 것으로 판명되었다. 즉 CTLA4가 제 역할을 못해서 면역계가 불필요하게 활성화 되어 자기 자신을 공격하는 자가면역 증세를 띠게 된 것이다. 운좋게도 이 단백질의 역할을 도와줄 수 있는 약이 있었으며, 실제 류마티스성 관절염에 쓰이고 있는 아바타셉트(Abatacept)라는 약제를 환자에게 투여, 실제 환자 돌연변이의 효과에 도움을 줄 수 있을지를 관찰하였고 그 결과 실제 아바타셉트가 실제 CTLA4의 역할을 도와주는 것으로 판명되었다. 임상적으로도 아바타셉트 투여 후 빈혈 증세가 빠르게 호전되어 빈혈은 완치 판정을 받았으며 설사 증세도 하루에 3리터에서 하루에 1리터 정도로 호전되는 결과를 관찰하였다. 이러한 증세 호전 덕분에 환자는 삼년간의 입원 생활을 마치고 통원 치료를 받고 있다 (그림 4).
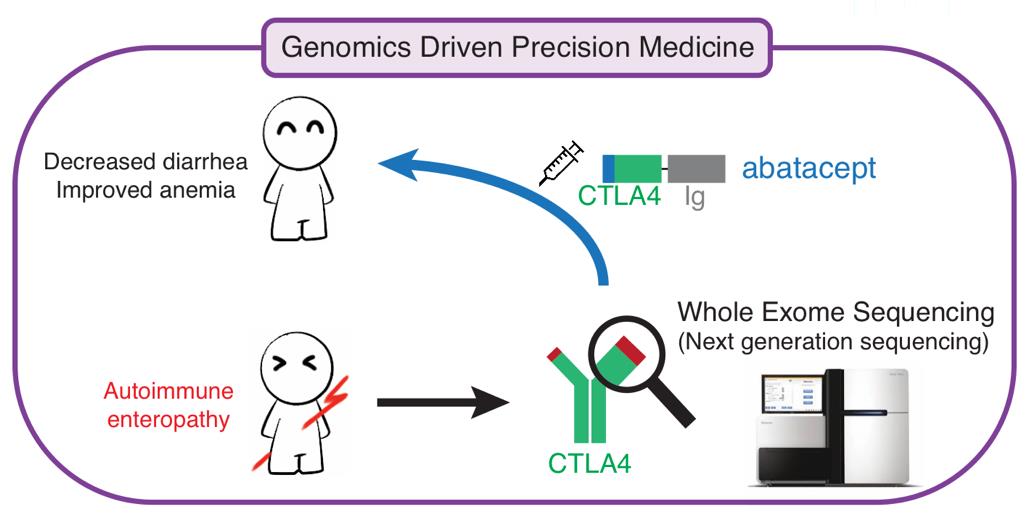
그림 4. 유전체학 방법으로 환자 특이적 돌연변이를 발견 한 후 그에 맞는 약제의 처방으로 환자의 증상 호전을 이뤄낸 연구 사례
본 연구는 미래 의학의 모델을 제시하였다. 즉, 환자가 병원에 오게 되면 그 환자의 유전체 분석을 통하여 그 병의 원인이 되는 돌연변이를 찾게 되고 이에 알맞은 적절한 치료법을 제시하는 모델이다. 이러한 맞춤의학의 예는 본 연구와 같이 희귀질환 모델에서 그 가치가 더욱 빛나며 더 효율적이다. 이 환자와 같은 자가면역 질환의 원인이 되는 새로운 타겟 유전자를 발견하였으며 이로 인한 새로운 면역적 반응 기작을 이해할 수 있었다.
5. 결론, 전망
빛은 색이 없다. 하지만 뉴턴 물리학은 그 이유를 이렇게 설명한다. 즉, 빛은 여러가지 색이 합성된 것이며, 이러한 상태를 프리즘을 이용하여 분산시키면 비로소 무지개와 같은 각종 색들이 나타나기 시작한다.
그림 5. 프리즘에 의한 빛의 분산
최신 차세대 염기해독법 (Next Generation Sequencing) 방법은 생물학, 의학을 망라한 여러 분야의 연구에 큰 변화를 일으키고 있으며 유전체학은 가장 큰 수혜를 입은 분야이다. 차세대 염기해독법을 적극적으로 이용하는 방법 중 하나가 전장 엑솜 염기해독법(Whole Exome Sequencing)이며 차세대 염기해독법 단가의 하락에 힘입어 전장 유전체 염기해독법(Whole Genome Sequencing)도 점점 널리 쓰이고 있다. 이와 같은 유전체학의 발전에 근거한 최근 미래 의학의 큰 화두는 개인 맞춤형 의학(Personalized Medicine), 정밀의학(Precision Medicine)이다. 실제 미 오바마 대통령은 작년 1월에 약 2천5백억 정도의 지원을 통하여 Precision Medicine Initiative를 발표하기도 하였으며 이 계획의 근간은 바로 유전체학이 될 것이다. 마치 프리즘이 빛을 분산시켜 그 본질을 볼 수 있게 해주는 것처럼, 기존의 의학으로는 쉽지 않았던 초희귀 질환 환자들의 진단과 병인 파악을 유전체학을 통하여 보다 정확히, 그리고 효율적으로 알아낼 수 있을 것이다.
6. 참고문헌
1. Alsalem et al. (2013) Autozygome sequencing expands the horizon of
human knockout research and provides novel insights into human phenotypic variation. PLoS Genet. 9:e1004030.
2. Chong et al. (2015) The Genetic Basis of Mendelian Phenotypes: Discoveries, Challenges, and Opportunities.
Am J Hum Genet. 97:1-17.
3. Gahl et al. (2016) The NIH Undiagnosed Diseases Program and Network: Applications to modern medicine.
Mol. Genet. Metabol. pii: S1096-7192.
4. Lee et al. (2016) Abatacept alleviates severe autoimmune symptoms in a patient carrying a de novo variant in CTLA-4.
J Allergy Clin Immunol. 137:327-330.
5. Sulem et al. (2015) Identification of a large set of rare complete human knockouts. Nat Genet. 47:448-452.
첨부파일